О применении электродиализа при судебнохимическом анализе алкалоидов
/ Вестфаль Н.И. // Судебно-медицинская экспертиза. — М., 1959 — №3. — С. 26-31.

Кафедра судебной химии (зав. — проф. М.Д. Швайкова) фармацевтического факультета I Московского ордена Ленина медицинского института имени И.М. Сеченова
За последние годы внимание исследователей все больше привлекает метод изолирования алкалоидов путем электродиализа. Этот метод может представлять интерес и для целей судебнохимического анализа.
Электродиализ можно характеризовать как процесс ускоренного переноса частиц, заряженных электричеством, через капиллярную структуру мембран. Введение -последних значительно усложняет процесс электролиза, поэтому нельзя представлять себе электродиализ как простую сумму двух процессов — электролиза и диализа. Большую роль играют также процессы перемещения воды и коллоидных частиц под действием тока (электроосмос и электрофорез).
Первые работы по практическому применению электродиализа были проведены в 1889 г. для очистки сахарного сиропа от следов электролитов.
Электродиализу подвергаются вещества неорганической и органической природы, диссоциированные в водных растворах, т. е. электролиты. Из органических веществ сюда можно отнести алкалоиды и органические основания, различные амины и аминокислоты, производные барбитуровой кислоты и т. д. Вещества с очень большой молекулой (например, белки) и электронейтральные вещества (например, сахар, желатина, некоторые антибиотики и др.) электродиализу не подвергаются.
Существенное влияние на ход электродиализа оказывают такие факторы, как материал электродов и мембран, рН среды, температура жидкости и т. д. При электродиализе алкалоидов особенно важно соблюдение условий температуры и рН, так как в ходе процесса температура жидкости имеет тенденцию к повышению за счет работы тока, некоторые же алкалоиды при одновременном воздействии нагревания и электрического тока могут изменяться.
Для целей токсикологического анализа электродиализ стал применяться сравнительно недавно. Литература в этой области не превышает 15 работ, главным образом французских.
Первыми такими работами можно считать работы Табона и Базиля (1935—1936) по изолированию арсената натрия, органических препаратов мышьяка, стрихнина, веронала и фтора из токсикологического материала. Авторы показали, что изолирование этих веществ путем электродиализа происходит быстрее и с меньшей затратой труда, чем при применении классических методов.
Фабр и Официальский изолировали стрихнин и веронал из 'биологического материала посредством электродиализа и показали, что этот метод исключает образование эмульсий и позволяет изолировать алкалоид из объектов, богатых липоидами.
Марик и Роша предложили усовершенствованный аппарат для работы с биологическим материалом.
В отечественной литературе были опубликованы co я С. Л. Архангеловой об опытах применения электро диализа для целей — токсикологии и высказаны соображения в пользу применения электродиализа как метода, давшего хорошие результаты.
И. В. Соколова сообщала об электродиализе биологического материала, смешанного со стрихнином, и материала из отравленных животных. Продукты, полученные в результате изолирования, исследовались качественной реакцией на стрихнин (с бихроматом калия в концентрированной серной кислоте). По мнению автора, качественное определение стрихнина, выделенного этим методом, возможно лишь при использовании не менее 5 мг его. В работе не приведена методика электродиализа и не дана количественная оценка результатов.
В 1955—1957 гг. в иностранной литературе появились работы по токсикологическому применению злектродиализа. Об изолировании из крови хинина и стрихнина сообщил Прейсс. Несколько позднее он предпринял попытки изолировать из биологического материала барбитураты электродиализом. Об опытах по применению электродиализа для целей токсикологии сообщила в 1957 г. Колянкевич. Интересна работа французского исследователя Молля. Автор применил электродиализ для изолирования ряда веществ, в том числе алкалоидов, из различных объектов, причем в тех случаях, когда классические методы анализа очень сложны или бессильны, метод электродиализа оказывается вполне удовлетворительным, например, при изолировании алкалоидов из объектов, богатых жирами, содержащих сахар, смолы и т. п.
В настоящей работе мы ставили перед собой задачу изучить метод электродиализа на примере алкалоида, имеющего токсикологическое значение, и попытаться разработать методику электродиализа для изолирования этого алкалоида из судебнохимических объектов.
В качестве примера алкалоида мы использовали стрихнин. Выбор основывался на следующих соображениях: стрихнин имеет токсикологический интерес, подвергается электродиализу сравнительно быстро, не претерпевая при этом химических изменений и, следовательно, мог слух жить хорошей моделью для изучения метода.
Нами был собран прибор, включаемый в цепь (постоянного тока (от выпрямителя тока), в цепь включали также измерительные приборы для контроля за режимом тока.
Изучив рекомендации различных авторов, мы нашли, что наиболее приемлемым для работы с судебнохимическим материалом может явиться прибор И. Е. Ласкина, который был нами несколько видоизменен. Взамен сетчатых электродов, закрепленных в крышке прибора, мы воспользовались плоскими, прямоугольными электродами, погруженными на дно сосуда (рис. 1). Каждый электрод предварительно был обернут в материал мембраны, наподобие мешочка так, чтобы на рабочей поверхности электрода находился один слой мембраны. Сосуд для электродиализа был стеклянный, объемом около 1 л, в нем находилась жидкость или соответствующим образом подготовленный объект, в катодное и анодное отделения наливали дистиллированную воду. Конструкция прибора создавала свободный доступ к любой части прибора в ходе работы, что было важно для исследований.
Для того чтобы выбрать оптимальные условия для изолирования стрихнина, мы вначале изучили процесс злектродиализа на его водных растворах, содержащих 1 мг нитрата стрихнина в 100 мл воды (стрихнин добавляли в виде 0,1 % водного раствора, предварительно проверенного количественно).
Оценку всех опытов проводили количественно, для чего был разработан колориметрический метод определения малых количеств стрихнина.
Мы изучали влияние на электродиализ материала электродов и мембран, рН и температуры жидкости, перемешивания ее и режима тока.
Дл я электродов проверяли следующие материалы: медь электролитическая, сталь нержавеющая (Марки ЭЯ-1Т), уголь электродный, графит подшипниковый (в различных сочетаниях попарно). Лучшие результаты были получены со стальным и графитовым электродами (соответственно катод и анод), с которыми мы проводили дальнейшую работу. Размер электродов 75X150 мм.
В качестве материала для мембран использовали пергаментную бумагу, целлофан и коллодий (удельный вес 0,76), с помощью которого были приготовлены мембраны по Бехольду: фильтровальную бумагу пропитывали коллодием, который затем фиксировали дистиллированной водой. Эти материалы мы проверили в различных сочетаниях. Наилучшие результаты дало применение пары мембран: пергаментная бумага — у катода, коллодиевая по Бехольду — у анода.
Относительно влияния рН жидкости на электродиализ в литературе имеются указания на то, что алкалоиды легче изолируются, если электродиализ ведется в кислой среде. Проверив влияние некоторых минеральных и органических кислот (соляной, серной, виннокаменной, щавелевой, уксусной), мы выбрали виннокаменную кислоту, которая обеспечивает достаточно кислую реакцию и не дает нежелательных вторичных продуктов при электродиализе. В ходе процесса рН жидкости контролировали капельным методом, предложенным Н. А. Тананаевым и А. Н. Тананаевым. Оптимальные условия рН, при которых следует вести процесс равны 5,5—6,5; такая кислотность достигается прибавлением 5—10 мл 100/о водного раствора виннокаменной кислоты.
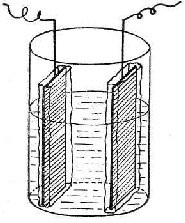
Рис. 1. Прибор для электродиализа.
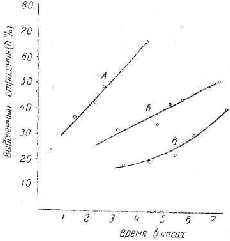
Рис. 2. Динамика изолирования стрихнина из его водных растворов электродиализом.
Оптимальные температурные условия при работе с биологическим материалом — не выше 40°, для этого необходимо внешнее охлаждение сосуда льдом или проточной водой. Следует отметить, что при работе с водными растворами повышение температуры жидкости не мешает изолированию стрихнина, но при работе с биологическим материалом нагревание влияет на проницаемость мембран, и при температуре выше 40° в католит могут переходить загрязняющие вещества.
Необходимо перемешивание смеси, особенно при работе с биологическим материалом. Мы осуществляли перемешивание путем барботирования пузырьков воздуха через смесь (от аспиратора).
Оптимальный режим тока — 60 V при плотности тока не более 10 mА/см.
На рис. 2 показана динамика изолирования стрихнина из водных растворов. Кривые обозначают изолирование стрихнина при оптимальных условиях с применением различных мембран: А — пергаментная и коллодиевая; Б — целлофановые; В —пергаментная и целлофановая.
Таким образом, мы установили условия, при которых за 6—8 часов удавалось изолировать от 80 до 100% стрихнина из его водных растворов. Такое время было намечено нами преднамеренно для того, чтобы не выходить из пределов оптимального времени, затрачиваемого на судеб- нохимический анализ алкалоидов.
В опытах с токсикологическим материалом объектом исследований служила печень. К измельченному объекту за 24 часа до опыта добавляли нитрат стрихнина в растворе и тщательно смешивали с объектом.
Изолирование путем электродиализа проводили в четырех вариантах в зависимости от порядка обработки объекта и применяемого растворителя (табл. 1).
Различные варианты изолирования стрихнина путем электродиализа
|
Объект исследования | Способ изолирования |
Добавлено стрихнина | Найдено стрихнина |
Время анализа |
Печень (100 г) То же » » » » | Электродиализ объекта, смешанного с водой Электродиализ объекта, смешанного со спиртом Электродиадиз водного извлечения из объекта (извлечение подкисленной водой) Электродиализ спиртового извлечения из объекта (извлечение подкисленным спиртом) |
2 2 2 2 | 1,6—14,6 3,8—5,1 2,6—8,4 3,0—7,1 | 4—7 5- 6 7—8 7—8 |
Как видно из табл. 1, общее количество изолированного алкалоида не превышает 15%. Наиболее продуктивным оказался электродиализ смеси измельченного объекта с водой.
Мы предлагаем следующую методику электродиализа стрихнина из биологического материала. Измельченный объект заливают 200 мл дистиллированной воды, добавляют около 5—10 мл 10% раствора виннокаменной кислоты (до рН 6), полученную смесь оставляют на 1—2 часа при частом -перемешивании. Затем смесь переносят в сосуд для электродиализа, в нее погружают электроды, обернутые материалом: мембран, в электродные мешочки наливают по 25—30 мл дистиллированной воды. Сосуд помещают в ванну с проточной водой или льдом, включают ток.
Электродиализ продолжается 6—8 часов, в течение которых необходимо контролировать температуру и уровень жидкости в приборе. По окончании процесса выключают ток, сливают катодную жидкость в делительную воронку и извлекают ее хлороформом.по 5 мл 3—4 раза. Реакция среды католита всегда резко щелочная, поэтому дополнительного подщелачивания не требуется. Хлороформные извлечения отделяют от водного слоя, фильтруют через сухой фильтр в фарфоровую чашку и хлороформ оставляют испаряться при комнатной температуре. Остаток от испарения хлороформа испытывают качественной пробой на стрихнин, а также определяют количественно.
Остатки в чашке, получаемые при работе с биологическим материалом, слегка окрашены в желтоватый цвет, имеют слабый ароматический запах, не кристаллические.
Анодную жидкость исследованию не подвергают, так как стрихнин в силу своей химической природы перемещается только к катоду.
Как уже отмечалось, количество стрихнина, изолируемое элек- гродиализом из биологического материала, весьма невелико. В связи с этим возник ряд вопросов о возможных причинах потерь алкалоида.
С целью их выяснения мы провели несколько серий опытов по сравнительной оценке трех методов изолирования стрихнина: электродиализом, подкисленной водой и подкисленным спиртом (табл. 2). Результаты опытов представлены в табл. 2.
Сравнительная оценка методов изолирования стрихнина
| Метод изолирования | Объект исследования | Добавлено стрихнина (в мг) |
Найдено стрихнина | Время анализа (в час.) |
Расход растворителей | |
| в мг | в % | |||||
| Подкисленным спиртом | Печень (100 г) |
2,0 2,0 |
0,18 0,175 |
9,0 8,7 |
180 190 |
250 мл спирта, 100-120 мл хлороформа |
| Подкисленной водой | Печень (100 г) Печень (100 г) Печень (100 г) |
3,0 4,3 7,8 |
0,14 0,775 0,88 |
7,0 18,0 11,3 |
6-8 6-8 6-8 |
250 мл спирта, 100-120 мл хлороформа
|
| Электродиализ | Печень (100 г) смешанная с водой |
2,0 3,0 4,0 |
0,032 0,44 0,28 |
1,6 14,6 7,0 |
4-5 7 6 |
20-25 мл |
| То же | Печень (100 г) смешанная со спиртом |
2,0 3,0 |
0,102 0,115 |
5,1 3,8 |
5-6 5 |
250 мл спирта, 20-25 мл хлороформа |
При сравнении трех методов изолирования видно, что результаты в среднем совпадают: количество изолированного любым способом алкалоида составляет около 7%.
Потери алкалоида при изолировании его из биологического материала, как правило, значительны, и в наших опытах электродиализ токсикологического материала не дал отклонений.
Какие же преимущества электродиализа мы можем отметить после некоторого изучения метода?
- Во-первых, значительная степень чистоты выделенного алкалоида, о чем говорит внешний вид остатков последнего после испарения хлороформа, а также отчетливая реакция стрихнина с бихроматом калия. Очистка алкалоида происходит одновременно с его выделением, дополнительной очистки не требуется.
- Во-вторых, метод электродиализа позволяет резко сократить расход органического растворителя (хлороформа) за счет легкости извлечения из католита, а также вследствие небольшого объема последнего (не более 100 мл).
- В-третьих, в ходе электродиализа алкалоид извлекается с помощью электричества, и рабочие руки требуются только для подготовки прибора и после выключения тока для обработки католита; з ходе процесса необходим лишь контроль за работой прибора.
Выводы
- Электродиализ является перспективным методом изолирования алкалоидов при судебнохимическом исследовании биологического материала.
- Существенное влияние на ход электродиализа алкалоидов оказывают: материал электродов и мембран, рН среды, температура жидкости, перемешивание и режим тока.
- Сравнительная оценка методов изолирования алкалоидов (на примере стрихнина) дает возможность считать, что методом электродиализа изолируется не меньшее количество алкалоида, чем при извлечении его подкисленным спиртом и подкисленной водой.
- Электродиализ обладает рядом преимуществ перед другими методами изолирования (значительная степень чистоты выделенного алкалоида, сокращение расхода растворителя — хлороформ, спирт; значительное сокращение рабочего времени химика).
похожие статьи
Перспективы использования параметров окислительной модификафии белков сыворотки крови для установления длительности агонального периода / Эделев И.С., Обухова Л.М., Андриянова Н.А., Эделев Н.С. // Судебная медицина. — 2019. — №3. — С. 28-32.
Обнаружение рокурония в биологических объектах методом высокоэффективной жидкостной хроматографии/масс-спектрометрии / Матвеева А.А., Федорова К.В., Лопушанская Е.М., Киреева А.В. // Судебная медицина. — 2019. — №2. — С. 49-51.
Изучение распределения неостигмина метилсульфата в организме теплокровных животных после внутрижелудочного введения / Алехина М.И., Шорманов В.К., Никитина Т.Н., Маркелова А.М. // Судебно-медицинская экспертиза. — М., 2019. — №2. — С. 40-47.
Обнаружение 25B-NBOMe — производного фенилэтиламина в биологическом материале / Барсегян С.С., Кирюшин А.Н., Ерощенко Н.Н., Туаева Н.О., Носырев А.Е., Кирилюк А.А. // Судебно-медицинская экспертиза. — М., 2019. — №2. — С. 34-39.
Особенности распределения 2,4- и 2,6-ди-трет-бутилгидроксибензола в организме теплокровных животных / Шорманов В.К., Цацуа Е.П., Асташкина А.П. // Судебно-медицинская экспертиза. — М., 2019. — №1. — С. 36-42.