Скрининг лекарственных препаратов в крови методом высокоэффективной жидкостной хроматографии
/ Кокорина Н.О. // Мат. VI Всеросс. съезда судебных медиков. — М.-Тюмень, 2005.

(Новосибирск)
Основной задачей в судебно- химическом анализе является идентификация лекарственного препарата в биологических объектах и определение его концентрации. В настоящее время основным методом анализа в судебной химии остается метод тонкослойной хроматографии (ТСХ), который неспецифичен, поскольку идентификация неизвестного лекарственного препарата эти методом часто неоднозначна из-за совпадения параметров, а иногда невозможна (1) и не дает количественного определения. Поэтому в настоящее время все более широко внедряются инструментальные методы анализа, обладающие высокой чувствительностью и избирательностью, а именно газовая хроматография с масс-селективным детектором (ГХ/МСД), высокоэффективная жидкостная хроматография с многоволновым детектированием (ВЭЖХ), капиллярный электрофорез (КЭ). Все эти методы можно использовать в скрининговом варианте.
В.А.Карташов и Л.В.Чернова (1998) разработали пять основных требований, которым должны удовлетворять скрининговые методы и разработали ТСХ и УФ-СФМ скрининговые методы (1). А.Б. Мелентьев (2003 ) предлагает скрининг наркотических и лекарственных препаратов и их метаболитов методом ТСХ и ГХ/МСД в моче, в которой концентрация вещества больше, чем в других объектах и наряду с нативными соединениями присутствуют их метаболиты (2). Однако пробоподготовка перед исследованием методом ГХ/МСД длительная и требует расхода дорогостоящих реактивов. Несомненным достоинством метода ГХ/МСД является наличие библиотеки лекарственных и наркотических препаратов и их метаболитов. Методы ВЭЖХ и КЭ не имеют подобных библиотек, но процессе работы их можно создавать самостоятельно
Нами в качестве скринингового метода предлагается использовать метод ВЭЖХ на высокоэффективном жидкостном хроматографе «Милихром А-02» (ЗАО «ЭкоНова» г. Новосибирск). на колонке 2х75 мм с обращено-фазовым сорбентом Prontosil120—5 С18, с многоволновым детектором. Элюенты: 0,1% раствор трифторуксусной кислоты в дистиллированной воде (элюент А) и 0,1% раствор трифторуксусной кислоты в ацетонитриле (элюент В). Градиент концентрации элюента В от 2 до 100 % за 3000 мкл. Скорость потока 150 мкл/мин. Рабочие длины вол детектора 220, 240, 250, 280 nm, базовая - 210 nm. Объем пробы 5-10 мкл. Идентификацию пиков проводили по временам удерживания и спектральным отношениям с использованием созданной нами библиотеки, включающей 240 лекарственных препаратов.
В практике работы нашего отделения для исследования методом ВЭЖХ, в том числе и для исследования в режиме скрининга, отдираются пробы объемом 0,6 мл из хлороформных экстрактов биообъектов, приготовленных как обычно для исследования методом ТСХ из кислого и щелочного раствора (3,4). Пробы из кислого и щелочного экстрактов объединяются, высушиваются на воздухе при комнатной температуре и сухой остаток растворяется в 0,2 мл 2% раствора ацетонитрила в 0,1% растворе трифторуксусной кислоты. Пробы готовятся в пробирках «Эппендорф». Объем исследуемой пробы 5-10 мкл. Таким образом, в одной пробе определяются вещества кислого и основного характера. Для определения концентраций лекарственных препаратов построены градуировочные графики по серии стандартных растворов методом абсолютной калибровки с использованием программного комплекса «Мультихром».
При определении лекарственного препарата в биообъектах, необходимо определить его концентрацию в крови, поскольку только для крови имеются данные по терапевтическим, токсическим и летальным дозам (5). Обычно используемая методика подготовки проб требует не менее 100 г (мл) биообъекта и включает жидкость-жидкостную экстракцию в делительных воронках, которая имеет множество недостатков, в том числе, плохую воспроизводимость. Поскольку для исследования методом ВЭЖХ необходимо всего 5-10 мкл пробы, была определена возможность проведения экстракции лекарственных препаратов кислого и основного характера из модельных смесей крови объемом 0,5 мл в пробирках «Эппендорф» .Модельные смеси готовили введением растворов лекарственных препаратов: азалептина, амитриптилина, анаприлина, димедрола, кофеина, фенобарбитала в концентрациях летальных и токсических доз. Модельные смеси крови выдерживали 2 суток и исследовали.
По 0,5 мл модельной смеси крови с лекарственными препаратами дозатором отбирали в пробирки «Эппендорф», дозатором по 10-50 мкл добавляли следующие реактивы: насыщенный раствор щавелевой кислоты, насыщенный раствор бикарбоната натрия, растворы аммиака, растворы серной кислоты. Пробы перемешивали и экстрагировали 0,5 мл хлороформа, выдерживая 30-60 мин в термомиксере при комнатной температуре и центрифугировали. Центрифугат отбирали шприцем, переносили в чистые пробирки «Эппендорф», из которых отбирали 0,3 мл пробы для исследования. Пробу высушивали на воздухе при комнатной температуре и растворяли в 0,15 мл 2% раствора ацетонитрила в 0,1% растворе трифторуксусной кислоты. Так же получили пробы модельной смеси крови экстракцией хлороформом из нейтральной среды, т.е. без изменения рН среды. Анализировали 5-10 мкл пробы. Регистрация и обработка хроматограмм проводилась с использованием программного комплекса «Мультихром».
Наилучшие результаты по проценту выхода всех введенных лекарственных препаратов получены при добавлении к модельной пробе крови насыщенного раствора щавелевой кислоты, насыщенного раствора бикарбоната натрия и экстракцией хлороформом без изменения рН среды (рис.1,2,3). Пики с временами удерживания были 6,28-6,38 мин – кофеин, 7,55 – 7,62 –азалептин, 8,308,34- фенобарбитал, 9,30-9,33- анаприлин, 9,81-9,85 димедрол, 10,95-11,06 амитриптилин.
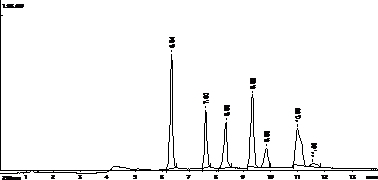
Рис.1 Хроматограмма хлороформного экстракта модельной смеси крови добавлением насыщенного раствора бикарбоната натрия

Рис.2 Хроматограмма хлороформного экстракта модельной смеси крови без изменения рН

Рис.3 Хроматограмма хлороформного экстракта модельной смеси крови добавлением насыщенного раствора щавелевой кислоты.
Также исследовали пробы модельных смесей крови после экстракции ацетоном и получили концентрации определяемых лекарственных препаратов не ниже, а в случае димедрола, выше, чем в пробах с насыщенным раствором м щавелевой кислоты, с насыщенным раствором бикарбоната натрия и пробе без изменения рН среды.
При проведении экстрагирования лекарственных препаратов из модельных образцов крови, разбавленных дистиллированной в соотношении 1:1, получены аналогичные результаты. По исследованным пробам отмечен воспроизводимый процент выхода лекарственного препарата.
Таким образом:
- Для идентификации лекарственных препаратов в режиме скрининга можно использовать метод ВЭЖХ, используя создаваемую базу данных лекарственных препаратов по временам удерживания и спектральным отношениям.
- Определения веществ кислого, основного и нейтрального характера возможно в одной пробе методом ВЭЖХ из пробы крови объемом 0,5 мл, что значительно снижает трудоемкость, затратность реактивов, сокращает случайные и систематические ошибки в процессе подготовки проб.
похожие статьи
Перспективы использования параметров окислительной модификафии белков сыворотки крови для установления длительности агонального периода / Эделев И.С., Обухова Л.М., Андриянова Н.А., Эделев Н.С. // Судебная медицина. — 2019. — №3. — С. 28-32.
Обнаружение рокурония в биологических объектах методом высокоэффективной жидкостной хроматографии/масс-спектрометрии / Матвеева А.А., Федорова К.В., Лопушанская Е.М., Киреева А.В. // Судебная медицина. — 2019. — №2. — С. 49-51.
Изучение распределения неостигмина метилсульфата в организме теплокровных животных после внутрижелудочного введения / Алехина М.И., Шорманов В.К., Никитина Т.Н., Маркелова А.М. // Судебно-медицинская экспертиза. — М., 2019. — №2. — С. 40-47.
Обнаружение 25B-NBOMe — производного фенилэтиламина в биологическом материале / Барсегян С.С., Кирюшин А.Н., Ерощенко Н.Н., Туаева Н.О., Носырев А.Е., Кирилюк А.А. // Судебно-медицинская экспертиза. — М., 2019. — №2. — С. 34-39.
Особенности распределения 2,4- и 2,6-ди-трет-бутилгидроксибензола в организме теплокровных животных / Шорманов В.К., Цацуа Е.П., Асташкина А.П. // Судебно-медицинская экспертиза. — М., 2019. — №1. — С. 36-42.