Применение трилона Б для определения кадмия в биологическом материале
/ Моисеева Т.М. // Судебно-медицинская экспертиза. — М., 1959 — №1. — С. 28-32.

Кафедра неорганической химии Рязанского медицинского института имени И. П. Павлова
Поступила в редакцию 6/Х 1958 г.
За последние годы в аналитической химии широко применяются, особенно при количественных определениях металлов,, так называемые «комплексоны» (а-аминополикарбоновые кислоты). Наибольшее распространение получила двунатриевая соль этилендиаминтетрауксусной кислоты, выпускаемой нашей промышленностью под названием «трилон Б» (за рубежом — комплексен III или версенат натрия).
По литературным данным, в настоящее время с успехом используются объемно-аналитические определения кадмия по специальным индикаторам при помощи раствора трилона Б.
В поисках пригодного для судебнохимических целей метода объемно- аналитического определения кадмия мы остановились на прямом титровании исследуемого раствора 0,01 М раствором трилона Б с применением в качестве индикатора сухой смеси азокрасителя — хромогена черного специального ET — 00 (эриохром черный Т) с хлоридом натрия в соотношении 1:200.
Принцип метода заключается в том, что хромоген черный специальный ЕТ-0 0 образует с кадмием интенсивно окрашенный в винно-краеный цвет комплекс (I), менее прочный, чем комплекс (IV) кадмия с трило- ном Б. В эквивалентной точке, когда все. ионы кадмия оказываются связанными трилоном Б (II) , возникает синяя окраска свободного хромогена черного специального ЕТ-ОО(Ш).
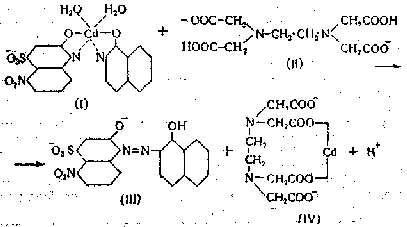
Процесс титрования проводится в щелочной среде при рН 10,0, что достигается применением аммиачного буфера1. Точка перехода окраски индикатора отчетлива даже при определении малых количеств кадмия.
Титр 0,01 М раствора трилона Б устанавливался нами по химически чистому металлическому цинку, из которого приготовлялся 0,01 М раствор хлорида цинка2.
Методика определения, которой мы пользовались, была следующей: к нейтральному раствору соли кадмия прибавляли аммиачный буфер из расчета 2 мл буфера на каждый 10 мл анализируемого раствора, затем небольшое количество сухой смеси индикатора (около 100—150 мг) и титровали жидкость раствором трилона Б до изменения окраски раствора от винно-красной до синей.
Метод был изучен нами на водных растворах я на растворах с применением общего хода судебиохимическосо анализа.
Результаты опытов, приведены в табл. 1.
Таблиц а 1
Результаты определения кадмия в водных растворах и в растворах по общему ходу судебнохимического анализа
№ п/п | Взято кадмия | Израсходовано |
Найдено кадмия | Величина отклонения |
Примечание | ||
|
в мг | в % | в мг | в % | ||||
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 | 10,02 10,02 6,01 5,01 2,00 2,00 1 ,00 1,00 0,50 0,50 0,50 10,00 10,00 10,00 5,00 5,00 6,00 2,00 2,00 2,00 | 9,65 9,7 4,85 4,8 1,95 1,93 0,98 0,97 0,47 0,49 0,48 9,45 9,5 9,3 4,7 4,75 4,6 1,7 1,85 1,8 | 10,00 10,04 5,02 4,97 2,02 2,00 1,01 1,00 0,49 0,51 0,50 9,88 9,94 9,73 4,92 4,97 4,81 1,78 1,93 1,88 | 99,8 100,2 100,2 99,2 101,0 100,0 101,0 100,0 98,0 102,0 100,0 98,8 99,4 97,3 98,4 99,4 96,2 88,0 96,5 94,0 |
—0,02 +0,0 2 +0,0 1 -0,0 4 +0,0 2 0 +0,0 1 0 —0,01 + 0,01 0 —0,12 —0,06 —0,27 —0,08 —0,03 —0,19 —0,22 —0,07 -0,1 2 | —0,2 +0, 2 +0, 2 -0, 8 +1, 0 0 +1, 0 0 —2,0 +2, 0 0 -1, 2 —0,6 —2,7 —1,6 —0,6 —3,8 —12,0 —3,5 -6, 0 |
Определение кадмия в водных растворах
1 мл 0,01 М раствора трилона Б соответствует 1,035 мг Cd2 +
В водных растворах по общему ходу судебнохимического анализа
1 мл 0,01 М раствора трилона Б соответствует 1,046 мг Cd2+-
|
Как видно из табл. 1, при определении от 10 до 0,5 мг кадмия в водных растворах ошибка определения колеблется в небольших пределах + 0,02— (—0,04 мг) и в процентном выражении + 2.
Если определение кадмия проводить в водных растворах по общему ходу судебнохимического анализа, наблюдается возрастание величины отклонения, что связано, очевидно, с потерями кадмия при различных операциях разделения. В абсолютном выражении величина отклонения для разных количеств кадмия примерно одного порядка, но в процентном выражении она увеличивается с уменьшением количества искомого элемента.
Получив хорошие результаты комплексометричеекого титрования кадмия на водных растворах, мы применили этот метод для определения кадмия в биологическом материале.
Следует отметить, что методы количественного определения кадмия в биологическом материале разработаны недостаточно, а объемные методы не применялись. Нами было проведено несколько серий опытов на мышцах, к которым добавлялось определенное количество кадмия, а также на паренхиматозных органах человека.
Биологический объект — 100 г — разрушался концентрированными серной и азотной кислотами. По окончании разрушения очислы азота удаляли при помощи формалина. Полученные жидкости исследовали по методике, описанной в руководстве по судебной химии А.В. Степанова (изд. 3-е) с внесенными нами следующими изменениями.
- Полученный минерализат усредняли раствором аммиака по индикатору метиловому фиолетовому до получения 0,3 N раствора (по свободной кислоте) и насыщали сероводором в течение 1 1/2 часов. Это изменение в общем ходе судебнохимического анализа позволяло сократить потери кадмия в процессе осаждения из минерализата в виде сульфида.
- После отделения от других веществ по ходу анализа осадок сульфида кадмия выделяли не фильтрованием, а центрифугированием. Предварительно мы установили, что при отделении сульфида кадмия фильтрованием волокна фильтра при дальнейшей обработке осадка соляной кислотой (1:3) переходят в раствор, а при выпаривании солянокислого раствора досуха на водяной бане остаток несколько обугливается. При растворении полученного остатка в воде и титровании раствора трилоном Б переход окраски индикатора становится нечетким, результаты количественного определения кадмия, как правило, в этих случаях получаются завышенными.
Из других катионов, отделяемых по ходу анализа, в титруемый раствор вместе с кадмием могут попасть только следы железы, что можно объяснить как процессами соосаждения естественно содержащегося в биологическом материале железа, так и введением его с реактивами например, с аммиаком). Наши опыты показали, однако, что соли железа в небольших количествах не влияют на результаты количественного определения кадмия комплексометрическим методом.
Таблица 2
Результаты определения кадмия в мышцах, к которым он был добавлен
|
№ | Взято | Израсходовано 0,01 M р-ра трилона Б (в мл) | Найдено | величина |
Примечание | ||
|
в мг | в % | в мг | в % | ||||
|
1 2 . 3 4 5 6 7 8 9 10 11 12 13 14 15 |
10,0 10,0 10,0 5,0 5,0 5,0 2,0 2,0 2,0 1,0 1,0 1,0 0,5 0,5 0,5 |
9,45 9,55 9,35 4,75 4,7 4,65 1,9 1,8 ' 1,85 0,85 0,9 0,95 0,35 0,3 0,4 | 9,88 9,98 9,78 4,97 4,92 4,86 1,99 1,88 1,93 0,89 0,94 0,99 0,37 0,31 0,42 | 98,8 99,8 97,8 99,4 98,4 97,2 99,5 94,0 96,5 89,0 94,0 99,0 74,0 62,0 84,0 |
—0,12 —0,02 —0,22 —0,03 —0,08 —0,14 —0,01 —0,12 —0,07 —0,11 —0,06 —0,01 —0,13 —0,19 —0,08 | 1,2 0,2 2,2 0,6 1,6 2,8 0,5 6,0 3,5 11,0 6,0 1,0 26,0 38,0 16,0 |
1 мл 0,01 М раствора.трилона Б
|
В табл. 2 представлены результаты опытов по определению кадмия в мышцах, к которым он был добавлен.
В слепых опытах — мышцы без добавления кадмия — последний по нашей методике никогда не обнаруживался
Анализируя данные табл. 2, мы видим, что сравнительно большие количества кадмия (10—5 мг) определяются довольно точно, величина отклонения колеблется в пределах от — 0,02 до — 0,22 мг, в процентном выражении от 0,2 до 2,8, тогда как при определении малых количеств кадмия (1—0,5 мг) потери, выраженные в процентах, увеличиваются примерно в 10 раз (от 1 до 38%) , несмотря на то, что в абсолютном выражении они примерно такие же (от 0,01 до — 0,19 мг), как и для больших коли- честв кадмия. Потери кадмия при исследовании биологического материала происходят не за счет метода количественного определения кадмия, а во время изолирования по общему ходу анализа.
Задача определения кадмия в биологическом материале, особенно при судебнохимических исследованиях, осложняется тем, что соединения этого элемента распространены в природе. По литературным данным, значительные количества кадмия содержатся в почках и печени человека, которые являются депо кадмия в организме. С возрастом в этих органах происходит накопление кадмия. Полярографическим анализом в почках человека обнаруживали 3,3 и 0,38 мг на 100 г сырого органа, данные же спектрального эмиссионного анализа показали среднее содержание в почках 1,6 мг кадмия на 100 г золы, а в печени — 4 мг Согласно другим данным, в почках печени людей, никогда не подвергавшихся воздействию кадмия, было обнаружено 3,31 и 0,36 мг Cd2 + на 100 г свежей ткани соответственно.
Таблиц а 3
Результаты определения кадмия в органах трупов человека
|
№ п/п | Возраст |
Название органа, взятого для исследования (100 г) |
Израсходовано 0,01 M р-ра трилона Б (в мл) | Найдено кадмия | Примечание |
|
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 | 60 54 51 50 41 24 19 12 64 54 50 40 45 24 60 60 51 51 | Почки » » » » » » » Печень » » » » » Кишечник Желудок с содержимым Кишечник Желудок без содержимого |
2,8 2,1 2,6 1,85 0,45 0 0 0,3 0,4 0,35 0,2 0 0 0 0 0 0 0 | 2,92 2,19 2,72 1,93 0,47 0 0 0,31 0,42 0,36 0,21 0 0 0 0 0 0 0 |
При проверке реактивов на содержание в них кадмия последний не обнаруживался
0,42 1 мл 0,01 М раствора трилона Б соответствует 1,044 мг Cd 2 +
|
В других внутренних органах человека содержание кадмия, сравнительно невелико. Возникла необходимость выяснить вопрос, будет ли определятья естественно содержащийся в органах человека кадмий ком- плекеометрическим титрованием при использовании измененной схемы общего судебнохимического анализа.
Для этой цели мы исследовали органы (печень, почки, желудок, кишечник) трупов людей различного возраста. Из 70 поставленных нами опытов в табл. 3 приводятся результаты отдельных определений. По нашим данным, наибольшие количества кадмия (от 0,47 до 2,92 мг) как биологического элемента определяется в почках. В печени содержание кадмия меньше и составляет всего 0,21—0,42 мг на 100 г органа.
В большинстве опытов естественно содержащийся кадмий в печени совсем не определялся. В желудке и кишечнике кадмий как биологический элемент по нашей методике ни в одном случае не обнаруживался3. Контрольный опыт с максимальным количеством реактивов также всегда давал отрицательные результаты.
Таким образом, при судебнохимичееком исследовании печени и почек человека следует осторожно давать заключение об обнаружении кадмия в названных органах, необходимо всегда производить количественное определение. Количества кадмия в печени менее 0,5 мг и в почках менее 3 мг, определенные по рекомендуемой нами методике, следует относить за счет естественно содержащегося кадмия.
Выводы
- Для определения кадмия в биологическом материале применен метод комплексометрического титрования трилоном Б по индикатору — хромогену черному специальному ЕТ-ОО.
- Метод прост по выполнению, точен, позволяет определять кадмий п сравнительно широком диапазоне.
- Ошибка определения кадмия (при количествах его от 10 до 0,5 мг) в водных растворах колеблется в пределах ±2% . -
- Установлено, что при определении кадмия в биологических объектах происходят потери его в процессе изолирования по общему ходу судебнохимического анализа. Из 10—5 мг, добавленных, в 100 г биологического материала, определяется 99,8—97,8%, а из 1—0,5 мг — 99—62%.
- При исследовании печени и почек человека в отдельных случаях определяется естественно содержащийся в них кадмий, поэтому количественное определение кадмия в биологическом материале обязательно.
1 54 г NH C1 и 350 мл 25% раствора NH OH в 1 л буферного раствора.
2 Параллельно титр раствора трилона Б определялся нами и по соли кадмия CdSО4 * 1/3 Н2О, перекристаллизованной, и проверенной, на процентное содержание. Результаты определения такие же, как и в первом случае, но применение для этой цели металлического .цинка ввиду постоянства его состава удобнее, чем соли кадмия. От использования металлического кадмия мы отказались потому, что он является редкоземельным элементом и имеется не во всех лабораториях.
3 По обычной методике общего хода судебнохимического анализа (осаждение CdS из минерализата, разбавленного водой до 200 мл, без усреднения) естественно содержащийся кадмий определялся только в почках в количестве 0,26—2,09 мг на 100 г объекта.похожие статьи
Особенности распределения 2,4- и 2,6-ди-трет-бутилгидроксибензола в организме теплокровных животных / Шорманов В.К., Цацуа Е.П., Асташкина А.П. // Судебно-медицинская экспертиза. — М., 2019. — №1. — С. 36-42.