Установление HBsAg в пятнах крови на вещественных доказательствах методом твердофазного иммуноферментного анализа. Методические рекомендации
/ Первушина Е.А., Гусаров А.А., Копылов А.В., Первушин Ю.В., Рогова С.Ш. — 2012.

Авторы:
Заведующая судебно-биологическая отделением ГБУЗ СК БСМЭ кандидат медицинских наук Е.А. Первушина; заведующий отделением судебно-биологических экспертиз ФГБУ РЦСМЭ Минздравсоцразвития России, кандидат медицинских наук А.А. Гусаров; начальник ГБУЗ СК БСМЭ кандидат медицинских наук А.В. Копылов; заведующий кафедрой клинической лабораторной диагностики ИПДО ГБОУ ВПО «Ставропольская государственная медицинская академия» Министерства здравоохранения и социального развития РФ, профессор Ю.В. Первушин; ассистент кафедры клинической лабораторной диагностики ИПДО ГБОУ ВПО «Ставропольская государственная медицинская академия» Министерства здравоохранения и социального развития РФ, кандидат медицинских наук С.Ш. Рогова.
Рецензенты:
- Е.Х. Баринов - зав. учебной частью кафедры судебной медицины и права ГБОУ ВПО МГМСУ Минздравсоцразвития РФ , к.м.н., доцент, профессор РАЕ
- В.А. Калянов - и.о. завкафедрой судебной медицины ГБОУ ВПО Казанский ГМУ Минздравсоцразвития РФ
Рекомендовано к изданию Ученым советом ФГБУ «РЦСМЭ» Минздравсоцразвития России (протокол № 2 от 29.03.2012г.).
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ УЧРЕЖДЕНИЕ
«РОССИЙСКИЙ ЦЕНТР СУДЕБНО-МЕДИЦИНСКОЙ ЭКСПЕРТИЗЫ»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
125284 Москва, ул. Поликарпова, д. 12/13;
ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ УЧРЕЖДЕНИЕ ЗДРАВООХРАНЕНИЯ
СТАВРОПОЛЬСКОГО КРАЯ «БЮРО СУДЕБНО-МЕДИЦИНСКОЙ ЭКСПЕРТИЗЫ»
355000, Ставрополь, ул. Дзержинского, 70.
«Утверждаю»
И.о. директора ФГБУ «РЦСМЭ» Минздравсоцразвития России,
доктор медицинских наук
А.В. Ковалев
/ 29 марта 2012 г.
Установление HBsAg в пятнах крови на вещественных доказательствах методом твердофазного иммуноферментного анализа
(Методические рекомендации)
Москва 2012
ВВЕДЕНИЕ
В настоящее время, благодаря развитию иммуногенетики, гематологии, биохимии и ряда других теоретических дисциплин, судебно-медицинская экспертиза крови получила возможность пополнить систему признаков, используемых для решения задач идентификации личности. В связи с этим перспективно использование маркеров, приобретенных организмом в процессе жизни (антигенов, антител). В качестве одного из них может быть использован сывороточный антиген гепатита В (HBsAg).
В России в последние годы заболеваемость гепатитом В имеет устойчивую тенденцию к росту как по количеству заболевших, так и выявленных носителей. Заболеваемость острым гепатитом В (регистрируются практически только желтушные формы заболевания) в последние 20 лет возросла более чем в три раза, достигнув в 1997 году 36,3 на 100 тыс. населения. Для сравнения показатели заболеваемости гепатитом В в странах Скандинавии, Ирландии и Великобритании менее 1, а в Германии, Франции, Италии - 3-5 на 100 тыс. Средний уровень носительства вируса гепатита В в нашей стране составляет 2,7%. По данным Госкомсанэпиднадзора, только за последние 2 года число заболевших острой формой гепатита В составило 105128 человек, было зарегистрировано 247245 новых вирусоносителей, большинство из которых имеет серьезную патологию печени.
Развитие методов иммуноферментного анализа определило возможность установления HBsAg не только в жидкой крови, но и в пятнах крови на вещественных доказательствах. Нами был разработана новая медицинская технология для определения HBsAg в пятнах крови методом твердофазного иммуноферментного анализа с использованием отечественного набора реагентов производства НПО «Диагностические системы». Принцип метода заключается в том, что в результате количественного твердофазного ИФА образуется специфический иммунный комплекс, состоящий из иммобилизованных на поверхности лунок полистирольного планшета антител к HBsAg, содержащегося в исследуемом материале HBsAg и антител, меченых пероксидазой хрена. Данный комплекс выявляется посредством окраски с помощью раствора тетраметилбензидина, после чего в лунки полистирольного планшета вносят стоп-реагент. Регистрация результатов реакции осуществляется фотометрически на регистрирующем приборе при длине волны 450 нм с последующим вычислением критической оптической плотности.
Аналогов данного метода по выявлению HBsAg в пятнах крови за рубежом не имеется.
Показания к использованию
В связи с тем, что HBsAg в крови практически здоровых людей встречается сравнительно редко (1-4%), его можно отнести к числу «особых примет» - признаков, индивидуализирующих личность. Эта особенность HBsAg при использовании в практике судебно-медицинской экспертизы позволяет конкретизировать происхождение крови на вещественных доказательствах от лиц, проходящих по делу и ограничить число подозреваемых при обработке следственных версий.
МАТЕРИАЛЬНО-ТЕХНИЧЕСКОЕ ОБЕСПЕЧЕНИЕ
Используют оборудование и реактивы, стандартные для судебно-биологических отделений бюро судебно-медицинской экспертизы, а также:
Набор реагентов дли иммуноферментного определения поверхностного антигена вируса гепатита В в сыворотке крови человека «ДС-ИФА-Н BsAg-0,01» НПО «Диагностические системы» по ТУ 9398-091-05941003-2006 (Паспорт 2198, регистрационное удостоверение ФСР № 2006/03019), используемый в клинической практике для установления инфицирования вирусом гепатита В.
Промыватель (вошер от англ. wash - мыть) медицинский микропланшетный фирмы «Sanofi Dagnostics Pasteur» PW40 (Регистрационное удостоверение МЗ РФ №2003/211 от 28.02.2003 г.); ридер (от англ. read - читать, считывать) «Sanofi Dagnostics Pasteur» PR2100 (Регистрационное удостоверение МЗ РФ №2003/211 от 28.02.2003 г.) и инкубатор для микропланшет IPS-2 той же фирмы (Регистрационное удостоверение МЗ РФ №2003/211 от 28.02.2003 г.).
Ридер (от англ. read - читать, считывать) фотометр для микропланшетов «Zemfira» фирмы «Bio-RAD Laboratories. Inc., США» с принадлежностями (Регистрационное удостоверение Федеральной службы по надзору в сфере здравоохранения и социального развития ФС №2006/1979 от 12.12.2006 г.).
ОПИСАНИЕ
Пробоподготовка образцов
После установления наличия и видовой принадлежности крови вырезают фрагмент из объекта размерами 0,5x0,5 см, либо несколько вырезок из участка размерами 10x10 см (в зависимости от тактики экспертного исследования, характера и величины следов. Исследуемый материал заливают минимальным необходимым (без избытка) объемом физиологического раствора. Экстрагируют при температуре 4° С от 18 до 24 часов. Возможно использование приготовленной ранее для установления наличия и видовой принадлежности крови вытяжки из следов крови.
Ход работы
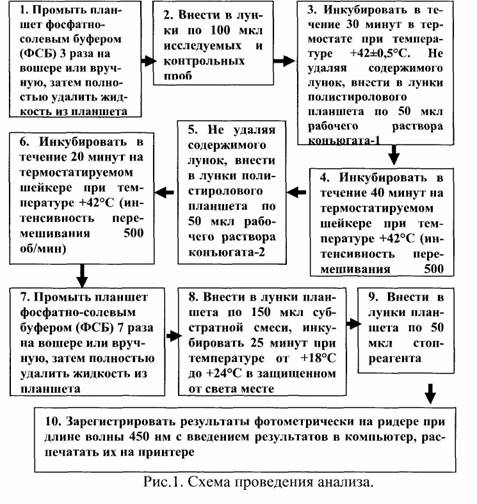
Данный метод реализовывался в следующей последовательности действий (рис. 1):
- - промывание перед использованием полистиролового планшета фосфатно-солевым буфером (ФСБ) с рН 7,2-7,4 3 раза на вошере (либо вручную) и полное удаление жидкости;
- - внесение в лунки полистиролового планшета по 100 мкл исследуемых и контрольных (отрицательной, положительной, слабоположительной) проб;
- - инкубация в течение 30 минут в термостате при температуре +42±0,5°С;
- - не удаляя содержимого лунок, внесение в лунки полистиролового планшета по 50 мкл рабочего раствора конъюгата-1 (моноклональные антитела к HBsAg, конъюгированные с биотином);
- - инкубация в течение 40 минут на термостатируемом шейкере при температуре +42°С (интенсивность перемешивания 500 об/мин);
- - не удаляя содержимого лунок, внесение в лунки полистиролового планшета по 50 мкл рабочего раствора конъюгата-2 (стрептавидин, конъюгированный с пероксидазой хрена);
- - инкубация в течение 20 минут на термостатируемом шейкере при температуре +42°С (интенсивность перемешивания 500 об/мин);
- - промывание фосфатно-солевым буфером (ФСБ) 7 раз на вошере (либо вручную) и полное удаление жидкости;
- - внесение в лунки полистиролового планшета по 150 мкл субстратной смеси (готовится непосредственно перед использованием путем разведения тетраметилбензидина (ТМБ), который представляет собой бесцветную жидкость на основе стабилизированного буферного раствора, содержащего 3,3 г, 5,5 г - тетраметилбензидина гидрохлорида, субстратным буферным раствором - цитратным буфером, содержащим раствор перекиси водорода);
- - инкубация 25 минут при температуре от +18°С до +24°С в защищенном от света месте;
- - внесение в лунки полистиролового планшета по 50 мкл стоп-реагента (1Н соляная кислота);
- - регистрация результатов реакции фотометрически на ридере при длине волны 450 нм с введением результатов в компьютер;
- - распечатка результатов с помощью принтера.
Оценка результатов
Компьютерную программу для ридера (программное обеспечение продается вместе с прибором, под каждый тест-набор пользователь сам или с помощью инженера-программиста составляет программу, исходя из инструкции к нему) следует написать так, чтобы отсечка шла от критической оптической плотности. Реакцию следует учитывать, если значение оптической плотности в лунках с положительным контролем не менее 0,6, а среднее значение в лунках с отрицательным контролем - не более 0,12.
Положительными считаются образцы со значениями оптической плотности, равными или превышающими критическую оптическую плотность, которая рассчитывается по формуле:
ОП крит. = ОП К'ср. + 0,06,
где 0,06 - коэффициент, определяемый методом статистической обработки результатов постановки ИФА на предприятии-изготовителе.
Контрольный слабоположительный образец, содержащий HBsAg в концентрации 0,02±0,01 МЕ/мл, должен давать положительную реакцию.
Исследуемые образцы расцениваются как отрицательные, если ОП образца < ОП крит.
Исследуемые образцы расцениваются как положительные, если ОП образца > ОП крит.
ЭФФЕКТИВНОСТЬ МЕТОДА
Эффективность использования метода заключается, прежде всего, в повышении качества судебно-медицинских экспертиз вещественных доказательств. Так, выявление в следах крови НЬ8А§ позволяет значительно повысить дифференцирующие возможности экспертизы.
Метод апробирован на заведомых образцах крови от 100 носителей HBsAg, высушенных на марле, при этом было исследовано около 500 объектов. Чувствительность реакции обнаружения HBsAg - 4x10 6 мл крови, при этом ложноположительных и ложно-отрицательных результатов зарегистрировано не было. HBsAg был обнаружен во всех исследованных пятнах крови, независимо от давности их образования. HBsAg не был обнаружен в пятнах крови лиц контрольной группы, а также в вытяжках из предмета-носителя.
Метод обладает рядом существенных преимуществ:
- Высокая чувствительность и специфичность в сочетании с объективной регистрацией и возможностью компьютерной обработки результатов. Документирование результатов ИФА в табличной форме позволяет дополнительно иллюстрировать заключения экспертов.
- Высокая воспроизводимость.
- Воздействие на кровь высокой температуры, прямых солнечных лучей, нахождение крови на снегу и почве, гемолиз не отражаются на результатах обнаружения НВsАg.
похожие статьи
Миокардиты Коксаки-B - вирусной этиологии как причина скоропостижной смерти детей раннего возраста / Гедыгушева Н.П. // Матер. IV Всеросс. съезда судебных медиков: тезисы докладов. — Владимир, 1996. — №2. — С. 25-26.
Метод избирательной абсорбции при определении кровяных групп в кровяных пятнах / Серебряников П. // Судебно-медицинская экспертиза. — М.: Изд-во Наркомздрава, 1928. — №8. — С. 3-7.