Обнаружение эфедрина и псевдоэфедрина в БАД
/ Сурнина О.В. // Избранные вопросы судебно-медицинской экспертизы. — Хабаровск, 2009 — №10. — С. 120-123.

98 Государственный центр судебно-медицинских и криминалистических экспертиз ДВО (начальник — И.П.Шульга)
В последние годы на территории Российской Федерации широкое распространение получил сбыт биологически-активных добавок сложного состава. Некоторые из них являются многокомпонентными смесями и содержат в себе составляющие растительного происхождения. Так при проведении экспертных исследований порошка из капсул БАД «для снижения веса и улучшения общего состояния организма» было установлено, что он является измельчённой разнородной массой из растительного сырья. Однако, при приеме в избыточном количестве от рекомендуемых в аннотации, появлялись признаки отравления эфедрином.
Эфедрин и псевдоэфедрин, относятся к алкалоидам растения эфедра.
Молекула эфедрина имеет два смежных ассиметрических атома углерода и может существовать в виде двух диастереомеров: эритро-формы и трео-формы, причём каждая из них является рацематом двух оптических изомеров: L и D. Таким образом, эфедрин и псевдоэфедрин – это диастереомеры одного вещества.
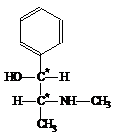 | 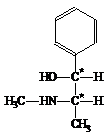 |
Псевдоэфедрин (трео-изомер) | Эфедрин (эритро-изомер) |
На организм эфедрин оказывает комплексное действие, стимулируя α- и β-адренорецепторы. При этом вызывает сужение сосудов, повышает артериальное давление, расширяет бронхи, тормозит перистальтику кишечника, расширяет зрачки, повышает содержание сахара в крови, возбуждает центральную нервную систему, повышает возбудимость дыхательного центра. Препараты, содержащие в своём составе эфедрин должны применяться только под наблюдение врача. Так как их бесконтрольное применение может вызвать ряд острых и хронических токсических эффектов.
Химическое исследование.
1. Метод ТСХ использовали для обнаружения эфедрина и псевдоэфедрина в измельчённой растительной массе. Экстракцию проводили этиловым спиртом, настаивали 30 минут, фильтровали и испаряли в токе тёплого воздуха до остатка 0,1 мл, наносили на хроматографическую пластинку с адсорбентом Сорбфил. Для целенаправленного ТСХ-анализа использовали ситемы: метанол-аммик (100:1), циклогексан-толуол-диэтиламин (75:15:10). Высушенные пластинки обрабатывали свежеприготовленным 1 % раствором нингидрина в ацетоне и нагревали в сушильном шкафу при температуре 90 0С в течение 5 минут. Значения Rf для эфедрина и псевдоэфедрина в первой системе - 0,29 и 0,32, во второй - 0,05 и 0,54, соответственно.
2. Методом ГХ-МС выполняли подтверждение полученного ранее результата. Хроматомасс-спектрометрию проводили на хроматографе Agilent 6890N с масс-селективным детектором Agilent 5973N фирмы Agilent Technologies (USA).
- Режим 1. Колонка HP–5MS длиной 30 м, с внутренним диаметром 0,25 мм. Газ-носитель – гелий, скорость газа-носителя в колонке - 1,0 мл/мин. Режим с делением потока в соотношении 1:20. Температуры: инжектора – 2800С, интерфейса – 2900С, начальная и конечная термостата колонки – 70 и 2800С, соответственно. Скорость изменения температуры колонки - 15 град/мин. Масс-спектрометр работал в режиме сканирования спектров электронного удара при 70 эВ диапазоне от 31 до 550 дальтон. Анализ проводили в режиме сканирования по полному ионному току. «Задержка на растворитель» время включения катодов и анализатора: через три минуты после ввода пробы. Диапазон масс: m/z 41-550 а.е.м. Напряжение на умножителе: результат, полученный при автоматической настройке по перфторбутиламину в режиме ATUNE.
- Режим 2. Отличается от предыдущего скоростью газа-носителя в колонке - 3,0 мл/мин и скоростью изменения температуры колонки - 30 град/мин.
Проведение реакции дериватизации (получения трифторацетильных производных). К упаренным экстрактам добавляли по 100 мкл хлороформа и трифторуксусного ангидрида, закрывали виалы завинчивающимися крышками с тефлонированной мембраной и выдерживали при 600С в течение 30 минут в термостате воздушной сушки. По окончании выдержки испаряли остатки реагента досуха слабым током азота. Остаток растворяли в 50 мкл обезвоженном сульфатом натрия безводном хлороформе. 1 мкл вводили в испаритель хроматографа.
Как на стадии подготовки и проведения реакции дериватизации, так и на стадии всего процесса анализа дериватов соблюдались меры по предотвращению попадания влаги в реакционную смесь, в том числе весь используемый хлороформ был осушен безводным сульфатом натрия, включая хлороформ, используемый для промывания шприца.
Из-за гидролитической неустойчивости дериватов, реакцию дериватизации проводили непосредственно перед анализами, а реакционную смесь после её упаривания немедленно анализировали.
Анализ полученных хроматографических данных проводился с использованием программного обеспечения «Hewlett-Packard G1540N MS ChemStation» и масс-спектрометрических баз данных библиотек WILEY 7 N, NIST 02, PMW-TOX 3, предоставленных фирмой-производителем. Хроматографический поиск осуществляли методом ручной обработки хроматограмм, а так же с применением стандартной системы поиска АМДИС.
Ниже на рисунках №№ 1 - 3 представлены фрагмент хроматограммы исследуемой массы по полному ионному току и масс-спектры обнаруженных 2-ТFA – производных эфедрина и псевдоэфедрина, которые сопоставимы с библиотечным данным # 3997: (Еphedrine 2 TFA с наиболее интенсивными ионами 56, 69, 91, 110, 127, 154, 244) и # 4016: (Рseudoephedrine 2 TFA с наиболее интенсивными ионами 56, 69, 84, 91, 110, 127, 154, 244). Вероятность совпадения с библиотечными данными составляла более 80 %.

Рис. 1. Фрагмент хроматограммы исследуемой массы по полному ионному току.
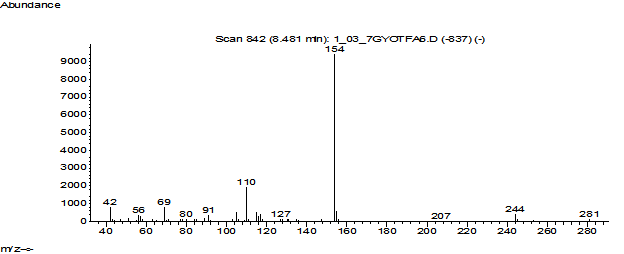
Рис. 2. Масс-спектр обнаруженного 2 ТFA – производного эфедрина в режиме № 1.
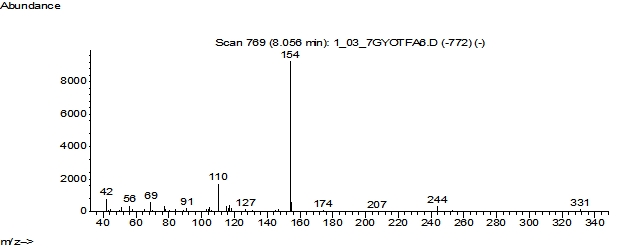
Рис. 3. Масс-спектр обнаруженного 2 ТFA – производного псевдоэфедрина в режиме № 1.
Метод газовой хроматографии с масс-спектральным детектированием является в настоящее время высокоспецифичным, чувствительным и достоверным. Точность идентификации достигается использованием масс спектра, высокой специфической характеристикой вещества. Данный метод хорошо зарекомендовал себя при проведении экспертных судебно-химических исследований и позволил подтвердить качественное обнаружение эфедрина в совокупности с псевдоэфедрином в представленной БАД.
похожие статьи
Перспективы использования параметров окислительной модификафии белков сыворотки крови для установления длительности агонального периода / Эделев И.С., Обухова Л.М., Андриянова Н.А., Эделев Н.С. // Судебная медицина. — 2019. — №3. — С. 28-32.
Обнаружение рокурония в биологических объектах методом высокоэффективной жидкостной хроматографии/масс-спектрометрии / Матвеева А.А., Федорова К.В., Лопушанская Е.М., Киреева А.В. // Судебная медицина. — 2019. — №2. — С. 49-51.
Изучение распределения неостигмина метилсульфата в организме теплокровных животных после внутрижелудочного введения / Алехина М.И., Шорманов В.К., Никитина Т.Н., Маркелова А.М. // Судебно-медицинская экспертиза. — М., 2019. — №2. — С. 40-47.
Обнаружение 25B-NBOMe — производного фенилэтиламина в биологическом материале / Барсегян С.С., Кирюшин А.Н., Ерощенко Н.Н., Туаева Н.О., Носырев А.Е., Кирилюк А.А. // Судебно-медицинская экспертиза. — М., 2019. — №2. — С. 34-39.
Особенности распределения 2,4- и 2,6-ди-трет-бутилгидроксибензола в организме теплокровных животных / Шорманов В.К., Цацуа Е.П., Асташкина А.П. // Судебно-медицинская экспертиза. — М., 2019. — №1. — С. 36-42.