Колориметрическое определение барбитуратов по интенсивности окраски виолуровой кислоты (на примере веронала)
/ Лобанов В.И. // Судебно-медицинская экспертиза. — М., 1963 — №1. — С. 39-44.

Поступила в редакцию 31/III 1962 г.
Количественное определение барбитуратов при судебнохимическом исследовании разработано еще недостаточно. В частности, при судебно-химических исследованиях до настоящего времени применяется малоэффективный и ненадежный весовой метод.
При определении барбитуратов широко применяется колориметрический метод, в основе которого лежит не специфичная для производных барбитуровой кислоты реакция Парри (Parri). Пфейль и Гольдбах (Pfeil, Goldbach) предложили меркурометрический метод, основанный на выделении нерастворимой ртутной соли барбитуратов. Последнюю разлагают с помощью кислоты, а освободившаяся ртуть образует с дитиозоном окрашенный раствор, который колориметрируют. Метод ненадежен, так как наряду с барбитуратами могут определяться вещества, образующие с ртутью нерастворимые соли. Похожий принцип положен в основу купрометрического определения производных барбитуровой кислоты (Л.И. Рапопорт); для выделения барбитуратов использован медно-пиридиновый реактив. За границей широко распространен спектрофотометрический метод количественного определения барбитуратов.
Таким образом, до настоящего времени нет метода количественного определения производных барбитуровой кислоты, основанного на специфичной для них реакции. Разработка такого метода особенно важна для судебной химии, так как объекты судебнохимического исследования бывают загрязнены веществами, дающими реакции на группировки атомов, содержащиеся в производных барбитуровой кислоты.
Целью данного исследования является разработка специфичной методики количественного определения барбитуратов, для чего использована разработанная нами ранее реакция качественного обнаружения производных барбитуровой кислоты.
В результате окисления барбитуратов и последующего восстановления полученного продукта образуется барбитуровая кислота. Конденсируясь с азотистой кислотой, она превращается в изонитрозобар- битуровую (виолуровую) кислоту, растворы которой имеют пурпурную окраску, причем интенсивность ее зависит от количества барбитурата.
Для исследования мы выбрали веронал, имеющий токсикологическое значение и широко применяющийся в медицине. Веронал можно превратить в барбитуровую и изонитрозобарбитуровую кислоту, в то же время он является одним из наиболее устойчивых в химическом отношении барбитуратов.
Было установлено, что интенсивность окраски растворов изонитрозобарбитуровой кислоты, полученной меньше чем из 10 мг веронала, слаба и не пригодна для колориметрирования. Поэтому разрабатывали методику для количеств от 10 до 100 мг. В 10 фарфоровых чашек диаметром 80—90 мм, на внутренних стенках которых имеется шкала с делениями не меньше чем на 0,5 мл, приливали соответствующие количества точно приготовленного 1% спиртового раствора веронала, с тем чтобы после испарения спирта в чашках осталось 10, 20, 30, 40, 50, 60, 70, 80, 90 и 100 мг веронала.
Исследуемые и стандартные растворы изонитрозобарбитуровой кислоты из веронала получали по следующей методике. К вероналу, оставшемуся в чашке после испарения спирта, прибавляли 1 мл 5% раствора хлористого натрия и 10 мл 30% пергидроля, помещали на кипящую водяную баню и нагревали до полного испарения жидкости. Остаток смачивали 10 мл 10% раствора перекиси водорода и повторно выпаривали на водяной бане.
Затем содержимое чашки опять смачивали 10 мл 3% раствора перекиси водорода и выпаривали еще раз, следя, чтобы на стенках чашки не образовался осадок, для чего содержимое периодически перемешивали. Каждое выпаривание заканчивали осторожно, чтобы не пересушить остаток, так как при этом он становился красным.
Получив продукты окисления всей серии, сухой остаток в каждой чашке растворяли при нагревании на водяной бане в 3 мл воды, прибавляя к нему из бюретки 1 мл раствора сульфида натрия1.
Приготовление раствора сульфида натрия. 100 мл 0,5 н. раствора едкого натра нагревают 15 минут от начала кипения с 5 г осажденной серы. Полученную желто-оранжевую жидкость фильтруют в мерную колбу на 100 мл и доводят водой до метки. Раствор годен в течение суток.
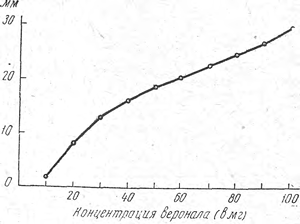
Рис. 1. Калибровочный график.
После прибавления раствора сульфида натрия жидкость нагревают на водяной бане 3 минуты и прибавляют к ней 1,1 мл 0,5 н. раствора соляной кислоты. Через минуту к содержимому чашки, не снимая ее с водяной бани, приливают 1 мл 10% раствора нитрита натрия и нагревают еще 3 минуты. Уровень жидкости в чашке к этому времени обычно бывает несколько ниже 3 мл (по шкале на внутренних стенках чашки). Если же окажется, что он превышает 3 мл, то нагревание ведут до тех пор, пока он не снизится, став несколько ниже 3 мл. После прибавления раствора нитрита натрия и нагревания жидкость окрашивается в пурпурный цвет. Чашку охлаждают и жидкость количественно переносят в градуированную центрифужную пробирку, где объем ее доводят до 3 мл водой и в течение 5 минут центрифугируют на суперцентрифуге при 10 000 оборотов в минуту. На дне пробирки собирается осадок серы, а над ней — прозрачный пурпурного цвета раствор, который затем пипеткой осторожно переносят в стаканчик для колориметрирования или химическую пробирку.
Растворы изонитрозобарбитуровой кислоты достаточно устойчивы и обычно сохраняются несколько дней.
Для измерения окраски этих растворов использовали концентрационный колориметр «КОЛ-1 М» (микростаканчики). При построении калибровочной кривой за стандартный принят раствор, соответствующий 60 мг веронала (рис. 1).
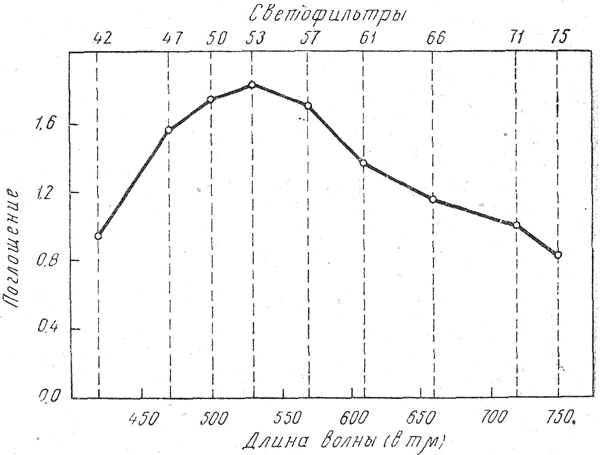
Рис. 2. График выбора светофильтра.
Верхние цифры обозначают номера светофильтров фотометра Пульфриха.
Как видно из кривой, наиболее пропорционально интенсивность окраски увеличивается на участке от 30 до 100 мг. Однако учитывая, что для судебной химии важны и малые концентрации, для работы использовали весь график. При помощи фотометра Пульфриха построили другой график (рис. 2), из которого видно, что количественное определение следует проводить, используя светофильтр Я = 530 тр.
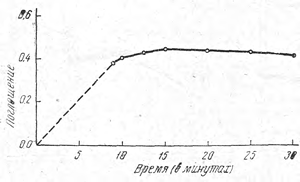
Рис. 3. Динамика реакции.
В процессе работы изучена динамика реакции. Так как появление и нарастание интенсивности окраски начинаются с момента прибавления нитрита натрия, после чего проводят еще нагревание и центрифугирование, изучение динамики начато с 9-й минуты после прибавления нитрита натрия. Из полученного графика (рис. 3) видно, что максимальной интенсивности окраска достигает на 15-й минуте.
Для проверки методики мы поставили ряд опытов, в которых брали точные навески веронала и проводили их количественное определение (табл. 1). Из таблицы видно, что абсолютная ошибка определения не превышает 0,005 г, а относительная (выраженная в процентах) при определении от 0,1 до 0,03 г составляет в среднем ±8%, а при определении от 0,03 до 0,01 г возрастает до ±18% и даже ±27%. По-видимому, это объясняется множеством превращений, которые претерпевает веронал ло получения изонитрозобарбитуровой кислоты.
Таблица 1
Веронал (в г) | Ошибка | ||
взято | найдено | абсолютная (в г) | относительная (в %) |
0,0960 0,0851 0,0924 0,0812 0,0707 0,0622 0,0561 0,0491 0,0410 0,0354 0,0282 0,0214 0,0166 0,0110 | 0,0910 0,0860 0,0900 0,0840 0,0680 0,0590 0,0580 0,0460 0,0380 0,0350 0,0260 0,0250 0,0120 0,0130 | —0,0050 +0,0010 —0,0024 +0,0028 —0,0027 —0,0032 +0,0019 —0,0031 —0,0030 —0,0004 —0,0022 +0,0036 —0,0046 +0,0020 | —5,20 +1,17 —2,61 +3,44 —3,96 —5,12 +3,10 —6.31 —7,31 —1,12 —7,80 +16,82 —27,71 + 18,18 |
Были поставлены опыты для установления возможности применения разработанной методики при количественном определении веронала, выделенного из биологического материала и мочи людей. К 100 г измельченной печени или почки добавляли определенные количества веронала и оставляли на сутки. По истечении указанного времени веронал извлекали подкисленным спиртом по методу Стасс—Отто, белкн осаждали, а водную жидкость экстрагировали эфиром. После испарения эфира остаток количественно исследовали на веронал.
Часть смеси биологического материала с вероналом экстрагировали подкисленной водой по методу А.А. Васильевой. Для этого 100 г измельченной почки или печени смешивали с определенным количеством веронала и оставляли на сутки, потом заливали водой и подкисляли щавелевой кислотой, после чего оставляли на 2 часа при частом помешивании. Водный экстракт сливали, фильтровали через складчатый фильтр и кислую водную жидкость несколько раз извлекали эфиром. Остатки воды из эфирного слоя удаляли центрифугированием. Полученный после испарения эфира остаток количественно исследовали на веронал.
Мочу исследовали следующим образом. 100 мл мочи смешивали с определенным количеством веронала и оставляли на сутки. Затем в случае нейтральной реакции ее подкисляли щавелевой кислотой и через 2 часа экстрагировали эфиром. Вытяжки промывали водой, остаток которой удаляли центрифугированием. Полученный после испарения эфира остаток количественно исследовали на веронал. Одновременно ставили контрольные опыты, в которых веронал к трупному материалу и моче не добавляли.
Таблица 2
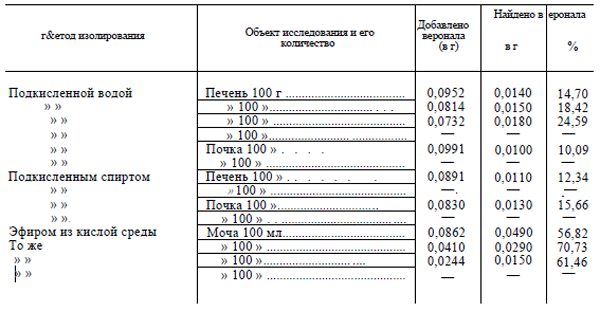
Результаты исследования приведены в табл. 2, из которой видно, что методика количественного определения веронала может быть применена как при исследовании внутренних органов, так и при исследовании мочи. «
Биологический материал не оказывал существенного влияния на химизм реакции, если не учитывать того, что часть веронала терялась за счет адсорбирования и в процессе изолирования.
Довольно часто объектом судебнохимического исследования бывают порошки и таблетки или их остатки. Для решения вопроса о возможности применения разработанной методики количественного определения веронала при исследовании этих объектов были поставлены опыты.
Порошки и таблетки получены в аптеке. Перед исследованием их взвешивали, затем таблетки измельчали в ступке. Навеску порошка или измельченной таблетки помещали в фарфоровую чашку и обрабатывали по описанной выше методике до получения окрашенного раствора изонитрозобарбитуровой кислоты. Окрашенные растворы колори- метрировали.
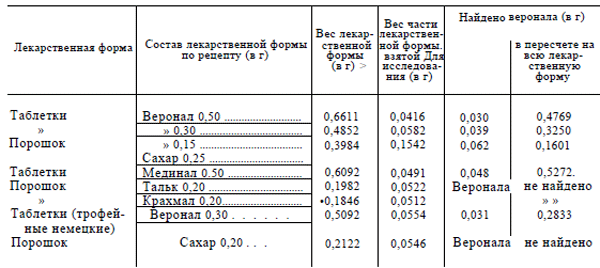
Результаты исследования приведены в табл. 3, из которой видно, что наполнители и вкусовые вещества, обычно добавляемые в порошки и таблетки, практически не мешают количественному определению веронала. Если исследовали порошки, не содержащие барбитуратов, то пурпурного окрашивания раствора не получали.
Определение веронала по предлагаемой методике можно проводить а интервале от 10 до 100 мг. Лучшие результаты получены при содержании веронала в исследуемом остатке свыше 30 мг.
Таблица 3
Нами установлено, что реакция образования изонитрозобарбитуровой кислоты протекает количественно с барбамилом, люминалом, нембуталом и тиопентал-натрием. На основании этого мы полагаем, что колориметрическое определение перечисленных барбитуратов можно осуществить после построения калибровочных графиков.
Разработка методики определения малых количеств барбитуратов (меньше 10 мг) продолжается.
Выводы
- Разработана методика колориметрического определения барбитуратов (на примере веронала), в основе которой лежит специфичная реакция образования изонитрозобарбитуровой кислоты.
- Разработанную методику можно использовать для определения барбитуратов, выделенных из биологического материала, а также при исследовании порошков и таблеток.
1 Р.Н. Копелиович рекомендует готовить раствор сульфида натрия кипячением 1 г серы с 10 мл 10% раствора едкого натра до получения интенсивно желтого цвета.
похожие статьи
Перспективы использования параметров окислительной модификафии белков сыворотки крови для установления длительности агонального периода / Эделев И.С., Обухова Л.М., Андриянова Н.А., Эделев Н.С. // Судебная медицина. — 2019. — №3. — С. 28-32.
Обнаружение рокурония в биологических объектах методом высокоэффективной жидкостной хроматографии/масс-спектрометрии / Матвеева А.А., Федорова К.В., Лопушанская Е.М., Киреева А.В. // Судебная медицина. — 2019. — №2. — С. 49-51.
Изучение распределения неостигмина метилсульфата в организме теплокровных животных после внутрижелудочного введения / Алехина М.И., Шорманов В.К., Никитина Т.Н., Маркелова А.М. // Судебно-медицинская экспертиза. — М., 2019. — №2. — С. 40-47.
Обнаружение 25B-NBOMe — производного фенилэтиламина в биологическом материале / Барсегян С.С., Кирюшин А.Н., Ерощенко Н.Н., Туаева Н.О., Носырев А.Е., Кирилюк А.А. // Судебно-медицинская экспертиза. — М., 2019. — №2. — С. 34-39.
Особенности распределения 2,4- и 2,6-ди-трет-бутилгидроксибензола в организме теплокровных животных / Шорманов В.К., Цацуа Е.П., Асташкина А.П. // Судебно-медицинская экспертиза. — М., 2019. — №1. — С. 36-42.