Обнаружение имменокса при химико-токсикологическом анализе
/ Саломатин Е.М., Шеенкова Г.Н. // Судебно-медицинская экспертиза. — М., 1974 — №3. — С. 43-45.

УДК 340.67:615.214.24:547.854.5
Научно-исследовательский институт судебной медицины (дир. — проф. В.И. Прозоровский) Министерства здравоохранения СССР, Московское городское бюро судебно-медицинской экспертизы (нач. — Л.С. Велишева)
Обнаружение имменокса при химико-токсикологическом анализе. Саломатин Е.М., Шеенкова Г.Е. Суд.-мед. эксперт., 1974, № 3, с. 43.
Изучены возможности идентификации имменокса микрокристаллическими реакциями, хроматографией в тонком слое сорбента и ультрафиолетовой спектрофотометрией. Разработан метод изолирования и обнаружения в трупном материале, использованный в экспертной практике. Иллюстраций 3.
Имменокс — 5-аллил-5-(1-метилбутил)-барбитуровая кислота (или барбитурат натрия) — снотворное лекарственное средство кратковременного действия итальянского производства. Выпускается в таблетках по 0,1 г. Терапевтическая доза —0,1—0,2 г. Высшая разовая доза — 0,4 г. Минимальная летальная доза — 2 г.
Это белый аморфный порошок, плохо растворимый в воде, хорошо растворимый в подкисленной воде, спирте, хлороформе, эфире и водных щелочных растворах. Температура плавления 100°. Натриевая соль препарата хорошо растворима в воде (1:3), спирте (1:5) и не растворима в эфире и хлороформе. Водные растворы обладают щелочной реакцией на лакмус.
Отмечены случаи отравления имменоксом. Wright установил, что концентрация имменокса в крови во время комы составляла от 1,9 до 5 мг%, а в период пробуждения — от 0,6 до 1,5 мг%; при смертельном отравлении концентрация в содержимом желудка была 0,13 мг%, в крови — 0,07, в печени — 0,25, в миокарде — 0,12, в мозге — 0,15, в жире — 0,4, в почке — 4,6 и в мышцах — 0,20 мг%.
В моче обнаруживаются незначительное количество неизмененного имменокса, а также его метаболиты.
Для идентификации имменокса в биологическом материале применяют хроматографию на бумаге и в тонком слое, газо-жидкостную хроматографию, УФ- и ИК-спектроскопию.
Случаи отравления имменоксом в нашей стране в судебно-медицинской практике не описаны.
Мы исследовали внутренние органы мужчины 35 лет, умершего после приема 4 г имменокса.
В литературе мы не нашли описания метода изолирования, обнаружения и определения имменокса в трупном материале, поэтому предварительно проверили отношение препарата к наиболее часто применяемым в судебно-химической практике реактивам на барбитураты.
С этой целью 25 мг имменокса извлекали хлороформом из водного раствора с рН 3—4 (по универсальному индикатору). После улетучивания хлороформа под микроскопом наблюдали кристаллический остаток — сростки бесцветных перистых кристаллов.
1. По данным Clarke, имменокс дает общую реакцию на барбитураты с солями кобальта. При проведении на фильтровальной бумаге общей на производные барбитуровой кислоты реакции окрашивания с 1% раствором нитрата кобальта в абсолютном метаноле с последующей обработкой парами аммиака наблюдали розово-фиолетовое пятно. В реакцию вводили 30—50 мкг препарата.
2. При перекристаллизации кислотной формы именнокса из концентрированной серной кислоты через 48 ч наблюдали сростки узких призматических кристаллов в форме сфероидов и обломки узких бесцветных кристаллов. В реакцию вводили 30—50 мг имменокса.
3. При микрокристаллических •реакциях как с железойодидной комплексной солью, так и с хлорцинкйодом образовались идентичные сростки из тонких призматических кристаллов в форме желтовато-серых сфероидов. Кристаллооптические константы микрокристаллов, полученных в результате взаимодействия с железойодидной комплексной солью, определяли с помощью поляризационного микроскопа. Микрокристаллы обладают плеохроизмом — по оси nР — черного, по оси ng — зеленовато-желтого цвета, кристаллы одноосны, погасание прямое, угол погасания 0°, знак удлинения отрицательный. В реакцию вводили 10—20 мкг препарата.
4. На спектрофотометре СФ-4А установлен максимум абсорбции при 238—243 нм в боратном буфере (рН 11).
По данным Bradford и Brackett, имменокс в боратном буфере (рН 9,4) имеет максимум абсорбции при 240 нм, при концентрации препарата 1 мкг/мл и использовании кюветы с рабочим ходом в 1 см.
Clarke (1969) отметил, что при рН 10,0 5,5- и 1,5,5-замещенные барбитуровой кислоты имеют максимум абсорбции при 240 нм, а тиобарбитураты — при 305 и 255 нм. При рН 13,0 1,5,5-замещенные барбитуровой кислоты имеют максимум абсорбции при 240 нм 5,5-замещенные — при 255 нм, а тиобарбитураты — при 305 нм.
5. Для очистки и идентификации имменокса, извлеченного из трупного материала, определили Rf при хроматографировании в тонком слое силикагеля ЛСЛ254 5/40 мк. Хроматографировали на пластинке 9×12 см со слоем силикагеля, забуференным 0,1 н. раствором борной кислоты (3,0 г силикагеля и 8 мл 0,1 н. раствора борной кислоты). Пластинки подсушивали и активировали при 100—105° в течение 30 мин. Имменокс и некоторые его аналоги хроматографировали в системе растворителей: хлороформ — н-бутанол — аммиак (75:40:5). Фронт растворителя — 10 см. Проявитель — 2,5% раствор сульфата 2-валентной ртути и 0,02% раствор дифенилкарбазона. После проявления пятно имменокса по краям было синего битала и люминала окрасились в фиолетовый цвет. Результаты приведены в таблице.
Из внутренних органов имменокс изолировали методом А.В. Васильевой. Имменокс дважды (2X60 мл) извлекали из кислой среды (рН 3—4) хлороформом. Подкисление объекта необходимо для лучшего растворения, а также для проведения гидролиза. Так, белковый комплекс альбуминовой фракции плазмы крови при рН 7—8 связывает 44% имменокса, что указывает на необходимость разрушения этого комплекса при изолировании препарата из биологических объектов.
Rf некоторых производных барбитуровой кислоты
|
Препарат |
Rf | |
|
полученная авторами |
по данным Н.В. Кокшаровой | |
|
Имменокс |
0,85—0,88 |
Нет |
|
Этаминал-натрий |
0,90 |
0,94—0,96 |
|
Барбамил |
0,87 |
0,85—0,92 |
|
Барбитал |
0,65—0,67 |
0,70—0,75 |
|
Фенобарбитал |
0,50 |
0,49—0,55 |
|
Квиэтал |
0,62 |
0,65—0,70 |
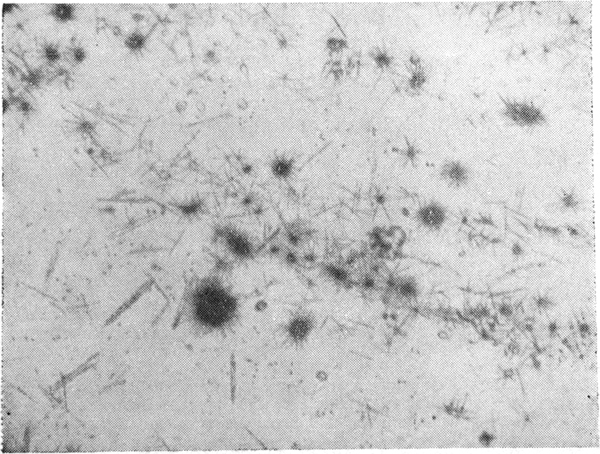
Рис. 1. Кристаллы имменокса, обнаруженные в желудке с содержимым. Ув. 80×.
По данным Turner, около 37% имменокса в крови после смерти связывается в белковом комплексе.
Все описанные выше реакции и методы были успешно использованы для доказательства имменокса, извлеченного из биологического материала, при исследовании указанного случая отравления (рис. 1, 2, 3).
Реакции с железойодидной комплексной солью и хлорцинкйодом позволили отдифференцировать имменокс от других барбитуратов.
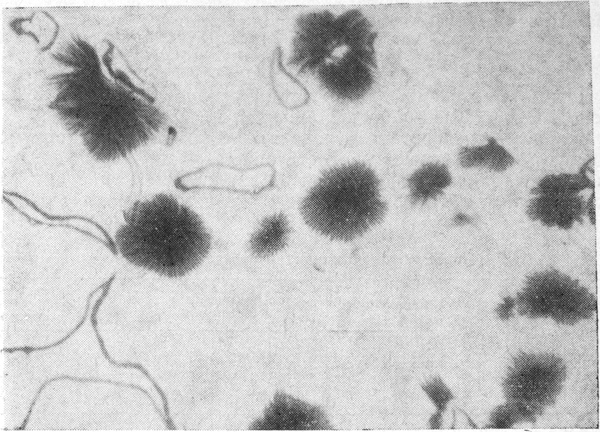
Рис. 2. Продукт взаимодействия выделенного из желудка имменокса с хлорцинкйодом. Ув. 240×.
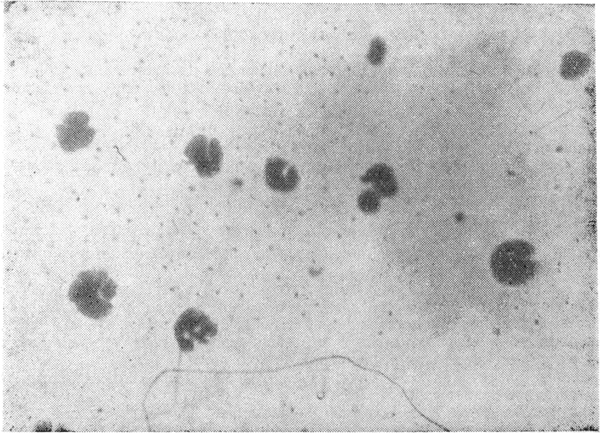
Рис. 3. Продукт взаимодействия выделенного из желудка имменокса с железойодидной комплексной солью. Ув. 240×.
Для определения максимума абсорбции имменокса, извлеченного из внутренних органов, необходима очистка от балластных веществ, так как они содержат естественные составные соединения организма (производные пиримидина), имеющие максимум абсорбции при 220—300 нм, что мешает идентификации имменокса.
Ввиду отсутствия кристаллического имменокса количественное определение не производили.
похожие статьи
Особенности распределения 2,4- и 2,6-ди-трет-бутилгидроксибензола в организме теплокровных животных / Шорманов В.К., Цацуа Е.П., Асташкина А.П. // Судебно-медицинская экспертиза. — М., 2019. — №1. — С. 36-42.