К вопросу о морфологии и физиологии органных сосудов в судебно-медицинском аспекте
/ Митяева Н.А., Науменко В.Г. // Судебно-медицинская экспертиза. — М., 1976 — №2. — С. 40-44.

УДК 611.13/. 16 + 612.131:340.6
Институт судебной медицины (дир. — проф. В.И. Прозоровский) Министерства здравоохранения СССР, Москва
К вопросу о морфологии и физиологии органных сосудов в судебно-медицинском аспекте. Митяева Н.А., Науменко В.Г. Суд.-мед. эксперт., 1976, № 2, с. 40.
Описано строение артерий запирательного типа, сосудистых анастомозов, клапанов и капиллярной сети; показано их функциональное значение в органном кровообращении.
Иллюстраций 4.
Особенности морфологии и физиологии органно-тканевого кровообращения во многом связаны с наличием так называемых приспособительных сосудистых образований.
В настоящей работе мы приводим сведения о замыкающих артериях, сосудистых анастомозах, клапанах и капиллярах, состояние которых необходимо учитывать при диагностике травмы, асфиксии, кровопотери и других экстремальных состояний.
Замыкающие сосуды обнаружены в артериальном русле всех органов и тканей. Замыкающими артериями их назвал А.В. Рывкинд (1948), запирательными — Науек (1953), а запирательными или толстостенными — Verloop (1948). На серии срезов можно видеть, что обычная артериальная ветвь внезапно теряет характерные черты строения стенки, просвет сосуда оказывается как бы заключенным в муфту из мощного слоя клеток. Мышечные клетки крупные, с прозрачной протоплазмой и округлым ядром, содержащим небольшое количество хроматина. Они часто приобретают полигональную форму, что вместе с прозрачностью цитоплазмы придает им сходство с эпителиальными клетками, поэтому их называют эпителиоидно-модифицированными клетками (Schumacher, 1938). Между мышечными клетками обнаруживается обилие тонких эластических волокон (в более крупных сосудах имеется еще наружная эластическая мембрана). Круговые мышечные волокна на этом участке чаще отсутствуют или слабо выражены; адвентиций отчетливый.
Наряду с типичными формами замыкающих артерий существуют их варианты. Например, в легких (А. В. Рывкинд, 1948; Verloop, 1948) и матке (Merkel, 1941) можно обнаружить сосуды, имеющие два слоя продольных мышечных волокон (внутренний и наружный), разделенных циркулярно расположенными мышечными клетками.
Участие артерий замыкающего типа в кровообращении весьма характерно для механической травмы, при этом оно имеет свои закономерности, помогающие определить время, прошедшее от момента травмы до наступления смерти. Артерии замыкающего типа входят в состав сосудистых анастомозов, в том числе артерио-венозных (А—В). Под термином А—В-анастомоз понимается соединение между артериальными и венозными сосудами [1]. В этом случае замыкающие артерии в определенном месте открываются в вены. По существу они являются артериальным сегментом анастомоза. Анастомозы могут быть простыми — короткими, с небольшим количеством эпителиоидно-модифицированных клеток, и сложными в виде клубочков с большим количеством такого же типа клеток, так называемые гломусы (Sherman).
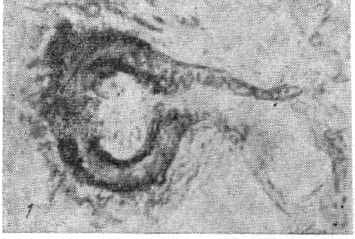
Рис. 1. Артерио-венозный анастомоз в легком.
Окраска фукселин-резорцином. Ув. ×400.
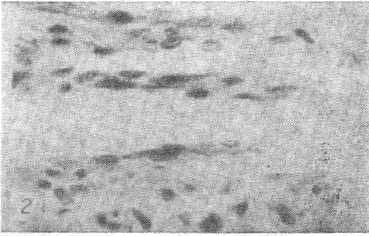
Рис. 2. Клапан по ходу вены в плевре.
Окраска гематоксилин-эозином. Ув. ×200.
Венозый сегмент А—В-анастомоза заметно отличается от обычных венозных сосудов соответствующего калибра. Это тонкостенный сосуд типа синусоида. Вблизи соустья он имеет элементы эпителиоидного типа, затем утрачивает их и стенка становится тонкой. Далее сосуд превращается в мелкую вену с обычной стенкой (рис. 1). Само соустье может располагаться в стенке замыкающей артерии или быть ее продолжением, его просвет по сравнению с просветом артериального и венозного отрезков почти щелевидный.
Экспериментальные и секционные данные показали, что А—В-анастомозы имеются не во всех органах и тканях. Так, в легких они располагаются только в стенках бронхов, перибронхиальной клетчатке и плевре (Merkel, 1941), а в веществе головного мозга и скелетной мускулатуре их нет (В. И. Козлов, 1972).
Во всех органах и тканях существуют анастомозы между мелкими артериями (А—А), между артериолами (Ал—Ал), между артериолами и венулами (Ал—Вл), между венулами (Вл—Вл) и между венами (В—В).
В венозных анастомозах в отличие от артериальных не выявлены структурные приспособления для активной регуляции кровотока.
Участие сосудистых анастомозов в ответной реакции на экстремальные воздействия наблюдается при странгуляционной асфиксии, что важно для ее диагностики.
К специализированным сосудистым образованиям венозного русла относятся клапаны. Они находятся на месте перехода крупных венул в мелкие вены (Ueoka, 1937), в венах толщиной 0,1—0,5 мк, где сосуд оказывается ампулообразно расширенным (устьевые клапаны). Клапаны имеются и по ходу более крупных вен. Их основу составляет волокнистая соединительная ткань — тонкая складка внутренней оболочки вены, покрытая эндотелием (рис. 2). Со стороны просвета сосуда эндотелий располагается продольно оси сосуда, а со стороны стенки — поперечно. В клапане имеются эластические волокна на стороне, обращенной к просвету, коллагеновые — на противоположной стороне, а у основания клапана находят мышечные волокна.
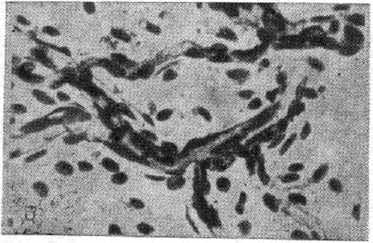
Рис. 3. Мелкоячеистая сеть капилляров в околопочечной соединительной ткани.
Импрегнация серебром по Компасу. Ув. Х600.
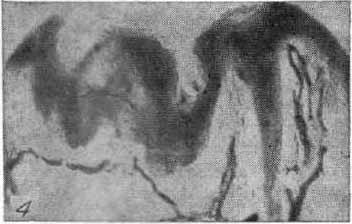
Рис. 4. Петлевидная сеть капилляров в коже спины.
Окраска по Шпнльмейеру. Ув. Х150.
Капиллярная сеть в различных органах и тканях разнообразна по плотности, рисунку ветвления (рис. 3 и 4) и диаметру сосудистых просветов (В.Г. Елисеев, 1963; Zweifach, 1954), что зависит от морфофункциональных особенностей тканей органов. В условиях физиологического покоя до 50% капилляров не функционируют, просвет их сужен, но не закрыт, он проходим только для плазмы (плазматические капилляры). Их считают переходной формой между функционирующими и нефункционирующими капиллярами (Г.И. Мчедлишвили, 1958). В органах и тканях имеются капилляры двух видов — очень тонкие, обеспечивающие питание органа, и магистральные, которые образуют анастомозы между артериолами и венулами и поддерживают механизм кровотока.
Регуляция кровотока в капиллярах определяется состоянием проксимального отрезка сосудистого русла и активной функцией самих капилляров. Krogh (1922) связывал механизм капиллярного кровотока с сократительной способностью перицитов. Это мнение разделяет Г.И. Мчедлишвили (1958). Перициты — клетки соединительнотканного происхождения, имеющие тончайшие отростки, которые они могут втягивать, при этом протоплазматическое тело утолщается. Существует мнение, что в пре- и посткапиллярах наблюдается постепенный переход от перицитов к мышечным клеткам. Установлена также способность эндотелиальных клеток набухать, за счет чего просвет капилляров может почти полностью закрываться (Д.А. Жданов, 1964; В.В. Куприянов, 1969; В.Н. Левин, 1970). Полагают, что набухание эндотелиальных клеток и «сокращение» перицитов происходит под влиянием гистамина и других медиаторов, которые появляются в тканях при нарушении кислотно-щелочного равновесия вследствие изменения функции. Кроме того, вокруг капилляров в строме обнаружены так называемые аргирофильные нити и кольца, которые, как предполагают, также способны суживать просвет (М. М. Александровская, 1955; Г. Г. Аминова, 1972).
Филогенетически сначала возникло общее кровообращение, затем — местное, в том числе капиллярное, которое появляется только с развитием тканей. Без капиллярного кровообращения нет и разделения на венозную и артериальную кровь. В онтогенезе сосудистая система также претерпевает ряд превращений, «отражая функциональные основы жизнедеятельности на различных этапах развития индивидуума» (И.В. Давыдовский, 1961). У новорожденных во многих органах и тканях имеется рассыпной тип сосудистого питания, когда широкие тонкостенные сосуды диффузно пронизывают паренхиму органа. Затем постепенно сосудистые стенки и ветви становятся более оформленными и сосуды располагаются менее густо. В дальнейшем сосудов становится еще меньше, появляется крупноствольный тип васкуляризации. В то же время у плодов количество артериальных ветвей, снабжающих кровью, в частности, трахею и бронхи, превосходит число аналогичных ветвей у детей; у них наблюдаются добавочные аркадообразные коллатерали, особенно вокруг желез подслизистого слоя (В.В. Куприянов, 1969).
В отношении А—В-анастомозов и артерий запирательного типа существует мнение, что у новорожденных они отсутствуют, но появляются вскоре после рождения (В.В. Рывкинд, 1948; И.В. Давыдовский, 1961). По нашим данным, А—В-анастомозы в легких формируются внутриутробно, а в функцию включаются с началом внеутробного дыхания не только у доношенных, но и у недоношенных. Они обеспечивают кровоток из сосудов большого круга в малый.
Клапаны начинают формироваться внутриутробно (В. Н. Пономаренко, 1965, и др.), и у новорожденных, и у детей первых месяцев жизни можно обнаружить уже полностью сформированные створки (см. рис. 2). Другие описанные ранее специализированные устройства в одних органах оказываются сформированными уже у плода и обнаруживаются при рождении, например артериальные «подушечки», «почки», замыкающие артерии в легких, «мышечные валики» в пупочных сосудах; в других органах появляются после рождения в ходе дифференцировки типа васкуляризации.
Специализированные сосудистые структуры — сосудистые анастомозы и клапаны — представляют собой функциональные приспособления системы местного, регионарного кровообращения. Анастомозирующие участки сосудистой сети — непостоянные пути кровотока. Они включаются временно в связи с функциональными потребностями ткани, выполняя роль шлюзов. Включаясь в кровоток при раскрытии сосудистого просвета запирательных артерий, они в одних случаях (А — В) обеспечивают внекапиллярный кровоток, который происходит в 3—5 раз быстрее капиллярного (В.В. Куприянов, 1969; В.И. Козлов, 1972), в других (А—А) — включение в кровообращение обособленных сегментов сосудистого русла, не функционировавших до этого. А—А- и Ал—Ал-анастомозы приводят к слиянию двух потоков крови, снижая давление в дистальных отделах сосудистого русла[3].
При закрытии просвета анастомозов (А—В, А—А) возникает обратное состояние. Анастомозы между венулами и мелкими венами, не имея запирательных устройств, не обеспечивают активной регуляции кровотока, они лишь дублируют путь оттока крови (В.И. Козлов, 1972).
Экспериментальные данные показывают, что артериальные анастомозы на уровне микроциркуляторной системы обнаруживаются не во всех органах и тканях, в частности их нет в скелетной мускулатуре. По-видимому, эти специализированные устройства имеются в тех органах и тканях, где сегментарная обособленность микроциркуляции обеспечивает непрерывную работу органа. У человека она, например, сегментарна в легких, париетальной плевре, брюшине. Каждый сегмент подобен другому и имеет артериолы, прекапилляры, капилляры, посткапилляры, венулы и Ал—Вл и другие соустья, т. е. все сосудистые компоненты местного кровотока (В. И. Козлов, 1972). Сегменты сосудистого русла, с одной стороны, представляют собой относительно изолированные фрагменты гемодинамической системы, и кровообращение в них определяется местными (органными) условиями метаболизма, а с другой – оно подчинено состоянию гемодинамики в целом. Приспособительные устройства типа замыкающих сосудов, раскрывая просвет, обеспечивают включение в кровообращение, а закрываясь — выключение из него целого участка — сегмента сосудистого русла.[2]
Замыкающие сосуды, как и другие приспособительные устройства, в некоторых органах имеются вне связи с сосудистыми анастомозами, при этом они служат для выполнения особых функций. Так, в пупочном канатике при его перерезке происходит сокращение кольцевой и продольной мускулатуры и полное закрытие просвета артерий, что препятствует потере крови; то же наблюдается в артериях матки после отделения плаценты. Таким образом, запирательные артерии в пупочном канатике и матке являются жизненно важными, охранительными приспособлениями. Влияние на организм в целом имеют запирательные устройства в венах надпочечников, где они регулируют отток адреналина.
Клапаны на уровне венулы — вены препятствуют обратному току крови; считают, что в момент кровотока на них действует присасывающая сила струи и их свободные концы стремятся к центру сосуда.
Приспособительные сосудистые механизмы используются организмом не всегда и не только целесообразно. Их реакция может быть на определенном этапе полезна, а затем становится фактором дальнейшего нарушения кровообращения. Так, за счет запирательных устройств при общем нарушении кровообращения может возникать венозный застой. Венозный застой постоянно сопутствует различным видам острой смерти, и при его оценке как проявления особенностей танатогенеза целесообразно учитывать состояние клапанного аппарата.
Формой адаптации сосудистой системы к потребностям тканей являются также различные состояния капилляров — их сокращение или расширение; помимо того, при повышенной функции в кровоток включаются почти все сосуды, а при пониженной в кровообращении участвует лишь минимальное их количество, необходимое для поддержания общего кровотока. При выключении из кровообращения части капилляров циркуляция осуществляется преимущественно по анастомозам.
Материалы о морфофункциональных особенностях на уровне органно-тканевого кровообращения будут изложены в следующей статье.
[1] Danesino (1948), Balestrazzi (1950), Sherman (1963) и другие авторы относят артерио-венозные анастомозы к прекапиллярным коммуникациям любого диаметра. А. В. Рывкинд, Verloop, Hayek, изучая легкие, находили их в сосудах диаметром не более 400 мк. Наш опыт исследования показывает правоту тех и других авторов; различия в их данных можно объяснить объектами (органами) исследования.
[2] С.И. Елизаровский и соавт. (1972), основываясь на результатах эксперимента, считают, что артериолярные соустья в условиях стрессовой ситуации суживают свой просвет не более чем на 10—20% исходного диаметра. По их мнению, эти сосуды выполняют роль связующего звена между артериальной и венозной системой, а не активного регулятора кровотока.
похожие статьи
Варианты составления описания, формулирования диагноза и выводов по основным видам повреждений / Исаков В.Д., Бабаханян Р.В., Белых А.Н., Колкутин В.В., Карнасевич Ю.А., Шандлоренко О.Н., Момот Д.В., Фетисов В.А. — 1997.