Газохроматографическое определение этилового спирта в выдыхаемом воздухе, слюне и моче человека
/ Степанов Л.Н., Терещенко А.П. // Судебно-медицинская экспертиза. — М., 1967 — №1. — С. 10-13.

УДК 615.711.12-099-07:616. 24-008.7+616-003.231+ 616-003.261]-074: 543. 544
Stepanov, L.N., Tereschenko A.P.: Gasochromatographic Ethyl Alcohol Estimation in the Expired Air, Saliva and Urine
Поступила в редакцию 26/III 1966 г.
В данной работе предпринята попытка определить этиловый спирт в выдыхаемом воздухе, слюне и моче человека. В процессе разработки методики исследовали также некоторые факторы, влияющие на содержание этилового спирта в биологических пробах.
Исследования проводили на газожидкостных хроматографах «Цвет-1» и «Shimadzu» С-IB с пламенно-ионизационными детекторами. В качестве газа-носителя (ГН) использовали гелий спецификации «В4» после дополнительной очистки на 2 последовательно соединенных колонках с силикогелем и молекулярным ситом 5А. Скорость газа-носителя (Vгн), водорода (Vн2 ) и воздуха (Vвозд.), температура колонок (tK), детектора (tД) и испарителя (tисп.), длина (l) и внутренний диаметр (d) колонок, неподвижная фаза (НФ) и твердый носитель (ТН) подбирали экспериментально.
В работе применяли 3 колонки:
I. НФ — полиэтиленгликоль (ПЭГ), молекулярного веса 6000; ТН — тефлон (фторопласт-4); l — 225 см; d = 0,4 см; II. НФ — полиэфирсукцинат (ПЭС); ТН — шималит; l=150 см; d = 0,4 см; III. НФ — смешанная, состоящая из 10% БЕТТА1БЕТТА1-оксидипропионитрила (ОДПН), 15% ПЭГ и 75% силиконового масла марки «ДС-550»; ТН — шималит; l = 250 см; d = 0,4 см. Размер зерен носителя аналитических колонок составлял 0,25—0,5 мм.
Пробу выдыхаемого воздуха отбирали стеклянным медицинским шприцем емкостью 5 и 10 мл, продувая его выдыхаемым воздухом. Летучие вещества мочи и слюны отбирали аналогичным шприцем из стеклянной колбочки емкостью 10 мл через самоуплотняющуюся резиновую пробку. Парогазовую фазу забирали после нагревания 1—2 мл жидкости на водяной бане.
Коэффициенты разделения (ацетон—этиловый спирт) для колонок II и III
Характеристика |
Колонка |
|
II |
III |
|
Сm1,2 |
16 |
7 |
Cmin1, 2 |
0 |
2 |
Q |
1 |
0,7 |
Анализируемую пробу вводили в испаритель шприцем при повышенной температуре. После каждого ввода шприц многократно промывали комнатным воздухом. Контроль чистоты шприца осуществляли путем сравнительного анализа промываемого воздуха с комнатным.
В процессе отработки методики определения этилового спирта изучали также некоторые другие легколетучие метаболиты. Пики этих веществ идентифицировали по времени удерживания и с помощью метода «меток». Пригодность колонок оценивали в экспериментах с выдыхаемым воздухом.
При сравнении хроматограмм выдыхаемого воздуха установлено, что степень разделения летучих метаболитов на 3 колонках различна. Коэффициенты разделения, найденные для II и III колонок по 2 соседним пикам (ацетон — этиловый спирт), представлены в таблице.
Коэффициент разделения (Q) определяли по формуле (3):
Q = (Cm1,2 -Cmin 1, 2) / Cm1,2
где: Сm1, 2 — среднее значение высот 2 пиков, Сmin 1, 2 — высота минимума между 2 пиками. Анализ данных таблицы и хроматограмм показывает, что лучшим разделением в условиях опыта обладает колонка II.

Рис. 1. Хроматограмма летучих метаболитов мочи человека. Колонка II; VГН= 50 мл/мин; t к =80°; tД =100°; tисп. =100°.

Рис. 2. Хроматограмма летучих метаболитов слюны человека. Колонка II; VГН =50 мл/мин; tK =80°; tД = 100°; tисп.. =100°.
К тому же вследствие небольшого времени удерживания (45 сек. ) пик этилового спирта выходит узким. Это облегчает расчет и идентификацию пика. Разделяющая способность колонки I выше, чем колонки II. В связи с этим, учитывая практическую направленность работы, в дальнейшем использовали колонку II.
После выбора колонки проверили возможность ее использования для определения этилового спирта в моче и слюне. Анализ хроматограмм (рис. 1, 2) показывает, что этиловый спирт из жидких биологических сред хорошо определяется на колонке II.

Рис. 3. Хроматограмма летучих метаболитов в выдыхаемом воздухе человека до и после курения. Колонка I; Vгн =30 мл/мин; tK =80° tД = 150°; tисп. = 100°.
Таким образом, предварительными исследованиями установлено, что колонку II можно использовать для определения этилового спирта в выдыхаемом воздухе, моче и слюне. Наиболее просто, удобно и быстро определять этиловый спирт в выдыхаемом воздухе. В связи с этим требовалось установить пределы возможных колебаний концентрации этилового спирта в выдыхаемом воздухе. С этой целью исследовали выдыхаемый воздух у 10 сотрудников. Содержание этилового спирта в выдыхаемом воздухе в течение дня (в относительных единицах) составляло соответственно: 3±0,1; 4±0,1; 2±0,1; 1,5±0,1; 1,7±0,5; 6±0,1; 5±0,1; 6,5±0,5; 7,5±0,5; 3±0,5. Представлялось целесообразным также установить влияние табачного дыма и кофе на выделение этилового спирта с выдыхаемым воздухом. Сравнительные хроматограммы в этом случае снимали через 1—2 мин. после выкуривания папиросы или 1—2 часа после принятия кофе.
После курения увеличивалось содержание в выдыхаемом воздухе легких углеводородов (преимущественно метана), ацетальдегида, ацетона и метилового спирта. Концентрация этилового спирта не повышалась (рис. 3). После употребления кофе увеличивалась величина пика, соответствующего метиловому и этиловому спиртам (рис. 4).
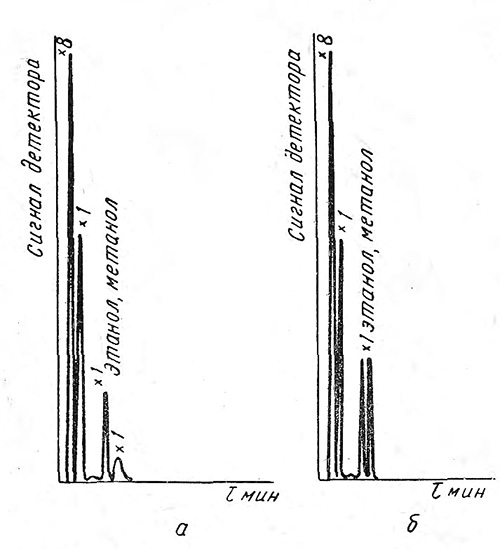
Рис. 4. Хроматограмма летучих метаболитов в выдыхаемом воздухе человека до (а) и после (б) употребления кофе. Колонка II; Vгн =30 мл/мин; t к =80°; tд =100°; tисп. =100°.
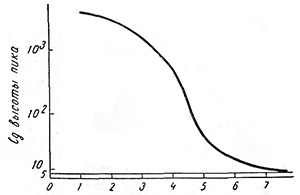
Рис. 5. Значения высот пиков этанола в выдыхаемом воздухе человека после употребления 100 мл 50% этилового спирта. 5 — эндогенный алкоголь.
Анализ полученных данных показывает, что содержание этилового спирта в выдыхаемом воздухе изменяется в широком диапазоне. В связи с этим представлялось целесообразным выяснить, через какое время концентрация этилового спирта в выдыхаемом воздухе человека, принявшего спирт, окажется равной фоновой. Полученная зависимость изменения высоты пика, соответствующего этиловому спирту во времени после принятия испытуемым спирта (100 мл 50% концентрации) (рис. 5), позволяет установить это время. Для данного случая оно равно примерно 6 часам.
Результаты определения этилового спирта в слюне и моче также показали, что повышенные концентрации можно определять через 4—6 часов после употребления этилового спирта. Так, в слюне содержание спирта через 4 часа после приема в 20 раз превышало таковое до опыта, в моче концентрация спирта через 6 часов была в 6—8 раз больше величины эндогенного спирта.
похожие статьи
Особенности распределения 2,4- и 2,6-ди-трет-бутилгидроксибензола в организме теплокровных животных / Шорманов В.К., Цацуа Е.П., Асташкина А.П. // Судебно-медицинская экспертиза. — М., 2019. — №1. — С. 36-42.