Некоторые вопросы изолирования и обнаружения кадмия в биологическом материале
/ Моисеева Т.M. // Судебно-медицинская экспертиза. — М., 1958 — №3. — С. 29-34.

Рязанский медицинский институт имени И. П. Павлова (дир. — проф. Л. Сутулов)
Поступила в редакцию 27/IV 1958 г.
Соединения кадмия представляют определенный интерес не только для врачей-токсикологов. В литературе описаны случаи отравлений кадмием как производственого, так и бытового характера, требующие проведения химического исследования. Однако методы судебнохимического исследования кадмия в объектах биологического происхождения недостаточно разработаны.
Для изолирования соединений кадмия из биологического материала нами был избран метод разрушения органических веществ концентрированными серной и азотной кислотами. Указанный метод разрушения имеет ряд преимуществ перед другими методами «мокрого» сжигания: довольно полное и быстрое разрушение органических веществ; получение малых объемов минерализата; быстрое удаление (при использовании денитраторов) остатков окислителя; достаточная чувствительность по отношению ко многим катионам и т. д.
Методика заключалась в следующем: 100 г тщательно измельченного биологического материала (мясо, печень и т. п.) обрабатывали в колбе Кьельдаля 75 мл смеси из концентрированных серной и азотной кислот и дистиллированной воды в отношении 1 : 1 : 1 и нагревали с периодическим добавлением (по мере надобности) по каплям азотной кислоты. Разрушение продолжалось до получения бесцветной (или почти бесцветной при отсутствии окрашенных ионов) жидкости, не темнеющей при нагревании в течение 30 минут без добавления азотной кислоты. Жидкость нагревалась до появления тяжелых белых паров серной кислоты. Остатки окислов азота удаляли при помощи формалина.
Таблица 1
Сравнительные данные осаждения CdS двумя способами
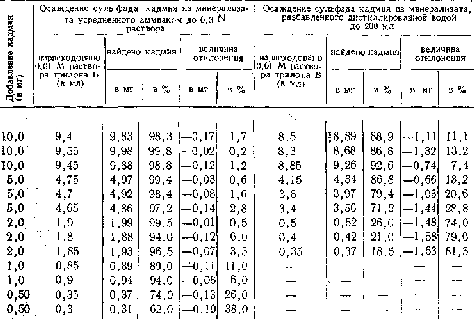
Примечание. 1 мл 0,01 М раствора трилона равен 1,046 мг Cd2+ . В качестве объекта исследования брали 100 г мышц, к которым добавляли определенное количество кадмия. В «слепых» опытах (100 г мышц без добавления соли кадмия) кадмий не Обнаруживался.
Из полученного минерализата по общему ходу судебнохимического анализа кадмий осаждался в виде сульфида. В результате опытов нами было установлено, что после разрушения 100 г биологического материала серной и азотной кислотами в среднем остается 20—22 мл 89% серной кислоты. После соответствующего разбавления дистиллированной водой до 200 мл, как это обычно рекомендуется при судебнохимических исследованиях, жидкость продолжает оставаться сильно кислой (примерно 4 N по свободной кислоте). Сульфид кадмия, как наиболее растворимый но сравнению с сульфидами других катионов IV и V аналитических групп, при этих условиях будет осаждаться не полностью. Для полноты осаждения кадмия нами рекомендуется сильно кислый минерализат после предварительного добавления 10—15 мл дистиллированной воды усреднять 25% раствором аммиака по индикатору — метиловому фиолетовому (водный раство р метилового фиолетового). При добавлении аммиака окраска раствора изменялась от желтой до светло-зеленой (но не голубой!), соответствующей 0,3 N раствору кислоты.
В табл. 1 приведены сравнительные данные количественного определения кадмия, полученные после осаждения сульфида его по общему ходу судебнохимического анализа.
Таблица 2
Результаты определения Сd2 + цианидным и тиосульфатным методами
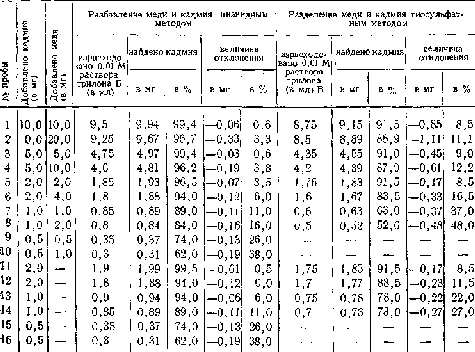
Примечание. 1 мл 0,01 М раствора трилона Б равен 1,046 мг.
Сульфид кадмия осаждался из минерализата, усредненного аммиаком до 0,3 N раствора кислоты, и из минерализата, разбавленного дистиллированной водой до 200 мл. После отделения от других катионов осадок сульфида кадмия растворяли в соляной кислоте (1 : 3), выпаривали досуха на водяной бане и остаток обрабатывали дистиллированной водой. Водные растворы после добавления соответствующего количества аммиачного буфера титровали 0,01 М раствором трилона Б по индикатору хромогену черному специальному ET-ОО в смеси с хлоридом натрия (1 : 200). Как видно из табл. 1, при определении сравнительно больших количеств кадмия, например 10 мг, в первом случае (осаждение сульфида кадмия из усредненного минерализата) теряется 0,2—1,7% кадмия, тогда как во втором — 7,4—13,2%. Малые количества кадмия (1—0,5 мг) определяются в первом случае в пределах от 62 до 94%, тогда как во втором из 2 мг кадмия, добавленных к 100 г биологического материала, определяется только 18,5—26%; при меньших количествах кадмий не определяется.
Таким образом, после осаждения сульфида кадмия из минерализата, усредненного аммиаком до 0,3 N раствора кислоты, результаты количественного определения кадмия значительно лучше, чем после осаждения сульфида кадмия из минерализата, разбавленного водой до 200 мл. В первом случае мы не только сокращаем объем минерализата почти, вдвое, но и повышаем границу определения кадмия в 4 раза.
При исследовании осадков сульфида кадмия по систематическому ходу анализа возникает необходимость в разделении меди и кадмия, так как, во-первых, эти элементы изолируются вместе, во-вторых, в качестве биологических элементов они могут присутствовать в исследуемом биологическом объекте. По литературным данным, в печени и почках человека находится наибольшее количество указанных катионов; так, в печени содержится (на 100 г золы) 4,02 мг меди и 4,06 мг кадмия, а в почках — 1,42 мг меди и 1,61 мг кадмия.
Таблица 3
Результаты обнаружения кадмия в биологическом материале по желтому сульфиду и контрольно-проверочным микрокристаллическим реакциям

Обозначения , + - положительный; 1- слабо положительный; — - отрицательный..
Классическим методом разделения меди и кадмия считается цианид- ный, описанный в руководстве А. В. Степанова. Так как этот метод требует применения ядовитого реактива, мы попытались использовать по отношению к биологическому материалу другой — тиосульфатный метод.
Методика разделения меди и кадмия тиосульфатным методом заключалась в следующем. Получаемый по ходу анализа аммиачный фильтрат, содержащий ионы кадмия и меди, нейтрализовали серной кислотой, смешивали с равным объемом 4 N серной кислоты для создания кислотности отвечающей 2 N кислоте. Жидкость переносили в центрифужную пробирку к нагревали до кипения в водяной бане. В горячий раствор вносили кристаллы тиосульфата натрия при помешивании жидкости и нагревании ее до выделения осадка Cu2S. Тиосульфат натрия добавляли до тех пор, пока от прибавления отдельного кристалла переставал выпадать черный осадок сульфида меди и начиналось более обильное выделение серы. Осадок Cu2S (частично и серы) отделяли центрифугированием; в центрифугат после добавления нескольких капель аммиака (до получения слабо кислой реакции) пропускали сероводород. Осадок сульфида кадмия отделяли и после соответствующей обработки кадмий определяли комплексометрическим титрованием.
Если объем фильтрата велик, его следует сгустить до малого объема.
В табл. 2. приведены результаты количественного определения кадмия после разделения меди и кадмия как цианидным, так и тиосульфат- ным методом. Объектом исследования служили 100 г мышц (пробы № 1—10), к которым добавляли определенное количество меди и кадмия, и 100 г печени (пробы № 11—16), к которой добавляли один кадмий. В «слепых» пробах (мышцы и печень без добавления названных катионов) естественно содержащийся кадмий не определялся.
Как видно из табл. 2, из больших количеств кадмия (10—5 мг), добавленных к биологическому материалу, после разделения цианидным методом определялось 99,4—96,2%, а тиосульфатным— 91,5—87,8%, из малых же количеств кадмия (1—0,5 мг) в первом случае определялось 89—62%, во втором из 1 мг определялось только 63—52%, а при добавлении 0,5 мг кадмия он вовсе не определялся. В пробах № 11 —16 кадмий отделялся от следов меди, естественно содержащейся в печени. Результаты определения кадмия в этих пробах несколько лучше, чем в пробах № 5—10, к которым прибавляли заранее определенное количество меди.
Необходимо отметить, что при определении в биологическом материале малых количеств кадмия (2 мг и менее) следует всегда производить разделение меди и кадмия, так как в этом случае кадмий отделяется не только от следов естественно содержащейся меди (если последняя обнаруживается в пробе), но и от следов железа, мешающих обнаружению малых количеств кадмия (получение вместо желтого осадка сульфида кадмия бурого). Следы этого элемента могут попасть в исследуемый раствор кадмия главным образом за счет процесса соосаждения естественно содержащегося в биологическом материале железа.
В руководствах по судебной химии для обнаружения кадмия рекомендуется только одна реакция — получение по общему ходу анализа желтого сульфида, нерастворимого в многосернистом аммонии. Хотя указанная реакция и считается наиболее характерной для иона кадмия, однако ввиду огромной ответственности судебнохимических анализов не следует давать заключение об обнаружении кадмия по результатам только одной реакции. Кроме того, в литературных источниках по аналитической химии имеется указание, что при избытке цианида калия под действием сероводорода иногда выпадает желтый осадок рубеанового водорода H2N—CS—CS—NH2 , который можно легко принять за сульфид кадмия. Для большей доказательности наличия кадмия в биологическом материале мы в целях проверки применили следующие микрокристаллические реакции: 1) образования комплексной соли кадмия с бруцином и бромидом калия; 2) образования комплексной соли кадмия с пиридином и бромидом калия и 3) образования двойной хлористой соли кадмия с цезием 1.
Раствор, полученный после растворения сульфида кадмия в соляной кислоте (1 : 3), выпаривали досуха. Остаток обрабатывали водой и с водным раствором проводили микрокристаллические реакции.
- К капле испытуемого раствора, нанесенного на предметное стекло, прибавляли каплю насыщенного раствора бруцина в 1 N серной кислоте и каплю 5% раствора бромида калия. В результате появлялись многолучевые розетки. Отдельные «глы розеток постепенно перерастали в ромбы и параллелограммы. Соединению кадмия с бруцином приписывается строение (C23 H26 O4 N2)2[Cd Br4]. Открываемый минимум — 0,33 у Cd 2 + при разведении 1 : 23 000.
- К капле исследуемого раствора, нанесенного на предметное стекло, добавляли каплю пиридина и небольшой кристаллик КВr — выделялись бесцветные характерные призматические кристаллы состава [Cd(CsH5N)4](CNS)2 . Открываемый минимум реакция — 0,13 у Cd 2 + при разведении 1 : 60 000.
- Каплю раствора соли кадмия выпаривали досуха, сухой остаток растворяли в капле соляной кислоты (1:1 ) и с края капли добавляли кристаллы CsCl. Выпадал осадок Cs4[CdCl6] в виде бесцветных квадратных и коротких призматических кристаллов. Открываемый минимум — 0,15 у Сd2 +при разведении 1 : 50 000 (табл. 3) .
Из табл. 3 следует, что в некоторых случаях при исследовании печени и почек человека «слепые» опыты (биологический объект без добавления кадмия) давали положительный результат, т. е. обнаруживался естественно содержащийся кадмий. При обычной методике осаждения сульфида кадмия из минерализата, разбавленного водой до 200 мл, кадмий как биологический элемент в печени никогда не обнаруживался, в почках обнаруживался в 62% случаев. При использовании методики осаждения сульфида кадмия из минерализата, усредненного аммиаком до 0,3 N раствора кислоты, кадмий обнаруживался в печени в 15% случаев, в почках — в 88 % случаев. Таким образом, при исследовании биологического материала, особенно таких паренхиматозных органов человека, как печень и почки, реакции качественного обнаружения иона кадмия без проведения количественного определения не могут иметь решающего значения при подозрении на отравление соединениями кадмия.
Выводы
- Усреднение сильно кислого минерализата аммиаком до 0,3 N раствора кислоты по метиловому фиолетовому позволяет производить осаждение сульфида кадмия при оптимальных условиях. При этом объем минерализата сокращается вдвое, а чувствительность определения кадмия повышается в 4 раза.
- Цианидный метод разделения меди и кадмия по систематическому ходу анализа более точный и простой, чем тиосульфатный. При отсутствии цианида калия в случае исследования биологического материала можно использовать тиосульфатный метод разделения.
- Для надежного обнаружения кадмия в объектах биологического происхождения сульфид кадмия, получаемый по общему ходу анализа, должен подвергаться проверке микрокристаллическими реакциями.
- При судебнохимическом исследовании тканей печени и почек человека с помощью качественных реакций обнаруживается естественно содержащийся кадмий.
- Для правильного заключения о нахождении кадмия в биологическом материале следует постоянно проводить количественное определение и давать оценку этому определению.
1 Реакции эти являются чувствительными и характерными на кадмий, но они не применялись при судебнохимических исследованиях.
похожие статьи
Редкая ошибка / Вонгродзский В.А. // Судебно-медицинская экспертиза. — М.: Изд-во Наркомздрава, 1928. — №8. — С. 116-119.
Изучение распределения неостигмина метилсульфата в организме теплокровных животных после внутрижелудочного введения / Алехина М.И., Шорманов В.К., Никитина Т.Н., Маркелова А.М. // Судебно-медицинская экспертиза. — М., 2019. — №2. — С. 40-47.